
扫码打开虎嗅APP

丙肝是肝癌的一个主要致病因素。全球约有7100万人感染丙肝病毒,世卫组织估计,2016年,约有39.9万人死于丙肝导致的肝硬化和肝细胞癌(原发性肝癌)。我国丙肝感染约有1000万例,中疾控数据显示,2019年新发病数有近22万。
好在,丙肝是可以治愈的。感谢科学家们几十年坚持不懈的努力,随着抗丙肝病毒特效药的问世,彻底消除丙型肝炎这一恶疾的目标已经有望实现。
今年的诺贝尔生理学或医学奖得主是发现丙型肝炎病毒的三位病毒学家。其中,第一位发现丙型肝炎的科学家阿尔特,在苦苦寻觅丙肝病毒的途中,曾呐喊道:请“肝神”指一条明路吧!
本文来自微信公众号:返朴(ID:fanpu2019),作者:何笑松(加州大学戴维斯医学院退休教授),原文标题:《肝神在上:谁能拯救七千万慢性丙肝病患?》,头图来自:视觉中国
2020年10月5日,诺贝尔奖委员会宣布,病毒学家阿尔特(Harvey J. Alter)、霍顿(Michael Houghton)、莱斯(Charles M. Rice)三人共同获得2020年的生理学或医学奖,获奖理由是“发现丙型肝炎病毒”。这是继1976年的乙型肝炎病毒诺贝尔医学奖之后,为第二种肝炎病毒的发现所颁发的诺奖。
病毒性肝炎是一大类常见病。感染肝脏、引起肝炎的病毒共有五型。这些病毒传染的途径和预后各不相同。五型肝炎中最常见的是甲、乙、丙三型,危害最大的则是乙型和丙型。甲型肝炎病毒通过粪-口途径传染,预后较好,绝大多数患者能自行清除病毒,完全康复,不会转变成慢性感染。乙型和丙型病毒通过血液和身体的密切接触传染。
成年人被乙型或丙型肝炎病毒感染后,相当一部分患者(乙型约10%,丙型约70%)转变为慢性肝炎,终身携带病毒。病毒携带者即使没有临床症状,仍可通过血液将病毒传给他人。乙型和丙型肝炎病毒的慢性感染大大增加了发生肝硬化,乃至肝癌等终末期肝病的风险,严重影响患者的健康和生命。
据世卫组织(WHO)估计,全球共有大约7100万慢性丙肝患者,2016年一年死于由丙肝病毒造成的肝硬化或肝癌人数近40万[1]。中国的慢性丙肝患者人数约为1000万[1,2] 。乙肝病毒危害的人数更是数倍于丙肝病毒。
由此不难理解,为什么乙肝和丙肝病毒的发现者都赢得了诺奖。虽然两种病毒的发现前后相隔二十年,二者发现的经过都充满了戏剧性。本文讲述关于丙肝病毒的故事,但这必须从乙肝病毒的发现说起。
19世纪末到20世纪上半叶是现代医学快速发展的黄金时期,注射器的发明、药物针剂以及输血和血液制品的推广使用,拯救了无数的生命。与此同时,医学界也注意到这些治疗措施有时会导致肝炎。病人接受输血后发生肝炎,成为临床上一个棘手的难题。据估计,20世纪中期,在美国接受输血后发生肝炎的比例曾高达30%。由于对引起肝炎的病原体一无所知,也就无从鉴别哪些供血者和血液样品带有传染性。为了防止发生输血后肝炎,寻找肝炎病原体已经成为刻不容缓的紧急任务。
就在此时,有两位科学家正关注着一项与肝炎风马牛不相及的研究。1964年,美国遗传学家布伦堡(Baruch Blumberg)与美国国立卫生研究院(NIH)一名年轻的研究人员阿尔特(Harvey J. Alter)开始合作,研究世界各地的不同人群中,由遗传因素造成的血清中所含蛋白质成分的差异。
他们发现,在一名澳大利亚土著居民的血液中,有一种独特的蛋白质,能被纽约市一名血友病患者的血清中所含的抗体识别。
血友病是一种遗传病,病人血液中缺少某些凝血因子,使得凝血功能受损,微小损伤即可造成严重出血。这些病人需要经常接受输血,或输入由血液制成的浓缩凝血因子来进行治疗。如果所接受的血液中含有病人自身的免疫系统从未接触过的异源蛋白质(抗原),病人就可能产生与之相应的特异性抗体。布伦堡将他新发现的这种蛋白质命名为“澳大利亚抗原”,简称“澳抗”。那个血友病人血清中所含的特异性抗体可以用来探测其它血液样品中是否存在澳抗。
美国的一般人群带有澳抗的比例不高,布伦堡对澳抗这种蛋白质的功能也一无所知。然而,两个偶然遇到的病例,将布伦堡的研究引向了一个全新的方向。
布伦堡的实验室中有个女技术员,工作中经常接触含有澳抗的血清样品。由于自己的血液中不含澳抗,因此她通常用自己的血清作为澳抗阴性的实验对照。1967年的一天,她感觉不适,而且出现黄疸症状,被诊断为肝炎。当她再次采集自己的血清来测定澳抗时,发现已从阴性转为阳性。另外一个病例是澳抗阴性的唐氏症患者,在被研究期间得了肝炎,澳抗也由阴转阳。布伦堡于是恍然大悟,将澳抗与肝炎联系起来。
与此同时,纽约血液中心有个叫普林斯(Alfred Prince)的研究人员,也利用来自一名接受过多次输血治疗的血友病人的血清抗体,在一批输血后肝炎患者的血液中找到一种与肝炎密切相关的新抗原,随后普林斯又发现,这种抗原就是已知的澳抗。
遗传学家布伦堡无心插柳柳成荫,一个华丽转身成为公认的肝炎病毒研究先驱, 并因此荣获1976年的诺贝尔医学奖。获奖理由是“发现澳大利亚抗原,并且证明它与血清性肝炎(输血后肝炎当时的名称)的联系”(尽管有人认为普林斯对证明这一联系的贡献比布伦堡更大)。
虽然此时澳抗的本质仍属未知——可能是导致肝炎的病原体(肝炎的原因),也可能是人体患肝炎后产生的反应(肝炎的结果)——但阿尔特已经敏锐地意识到,对供血者普遍进行澳抗的筛选,将有助于防止输血后肝炎。于是他开始为此发声呼吁[3]。
进一步的研究发现,澳抗就是乙型肝炎病毒的外壳蛋白质,它被正式命名为“乙型肝炎表面抗原”。紧随乙肝病毒之后,甲型肝炎病毒也被发现,相关的诊断试剂随之被开发出来,可以准确方便地鉴别出被甲肝、乙肝病毒感染的病人。尤其重要的是,乙肝病毒携带者可以没有任何肝炎临床症状,他们的血液如果被用于输血,就可能让接受者染上乙肝。在阿尔特与其同事的大力推动下,澳抗发现的短短几年后,全美所有的血库都对供血者实行了强制性的乙肝表面抗原筛选。
这一措施显著降低了输血后肝炎的发病率,但是并没有像人们期待的那样,杜绝输血后肝炎的发生。 最初,这被归咎于检测方法不够灵敏,血液中抗原浓度较低时可能漏检;但在新的检测方法大幅度提升灵敏度以后,输血后肝炎依然存在。
到了1970年代末,乙肝表面抗原发现的十年之后,阿尔特等人终于确定,除了乙型肝炎之外,还存在其它类型的肝炎,可通过血液传染。阿尔特笼统地称之为非甲非乙型肝炎,因为还不了解它的病因是一种,还是多种病原体[4,5]。研究人员不得不重振旗鼓,投入新一轮的探索。
有了发现两种肝炎病毒(特别是乙肝病毒)的成功经验在先,是不是就能驾轻就熟地找出非甲非乙型肝炎的病原体?
事实证明,没这么简单。
乙肝病毒的发现过程中最关键的一项突破,莫过于确定澳抗与输血后肝炎的联系。确定这种联系,依靠两个关键要素:已被发现的澳抗,和能够方便准确地探测到澳抗的抗体。可是对于非甲非乙型肝炎,研究人员对其抗原或抗体都一无所知,又该从何处着手?
尽管情况不容乐观,有一项重要进展还是带来了希望。阿尔特与NIH的同事普赛尔(Robert Purcell),以及美国疾控中心(CDC)的布雷德利(Daniel Bradley)等几个团队发现,将非甲非乙型肝炎病人的血清注射到最接近人类的灵长类动物——黑猩猩——体内,可以引发非甲非乙型肝炎,这表明黑猩猩可以作为非甲非乙型肝炎的实验动物模型。再以陶瓷滤器将病人血清中可能含有的细菌滤除,过滤后的血清仍然能使黑猩猩致病,这表明病原体应当是一种(或几种)比细菌小的病毒,而非细菌[6]。
阿尔特的首要目标是防止输血后肝炎的发生,为此必须找到一种方便灵敏的检验方法,可以清楚地区分正常血液和致病血液。可是他的团队用尽各种传统方法,不管是直接探测病原体,还是间接探测人体对病原体的免疫反应产物,都没有成功。
在此过程中,阿尔特收集整理了一套血清样品,其中有些来自感染了非甲非乙型肝炎的病人或黑猩猩,作为阳性的标准样品;另一些来自患有其它肝脏疾病的病人,作为阴性对照。每个样品有一个代码,只有他本人掌握解码的密钥。新开发的任何一种检验方法都必须经过这套标准样品的测试,准确地鉴别出其中所有的阳性和阴性样品,才能通过。
从1978年开始,十年间,先后有多个研究非甲非乙型肝炎检测试剂的团队,前仆后继地向阿尔特的这套标准样品发起了共约20次挑战,全都铩羽而归,无一例外。
1982年,出生于英国的病毒学家霍顿(Michael Houghton)移居美国,加入旧金山湾区新成立的凯荣(Chiron)公司,主持非甲非乙型肝炎病原体的研究。团队里有两位骨干,华裔博士郭劲宏(George Kuo)和朱桂霖(Qui-Lim Choo)。八十年代初,正是以重组DNA为代表的分子生物学研究方兴未艾之际,霍顿决定摒弃着眼于病毒的蛋白质产物的传统策略,另辟蹊径,采用基因克隆的方法,直接寻找病毒的遗传物质——核酸(DNA或者RNA)。
划时代的重组DNA技术是在上世纪七十年代初期诞生的。美国斯坦福大学的伯格(Paul Berg)成功地把分别来自两种不同病毒的两个DNA片段准确地拼接到一起,成为一个连续的重组DNA分子。一年后,伯格的同事科恩(Stanley Cohen)和加州大学的博耶(Herb Boyer)使用质粒构建重组DNA分子,把伯格的结果向前又推进一步。
质粒是大肠杆菌中常见的一种环状DNA分子,它独立于细菌染色体之外,可以自主复制(参见《啥是质粒?从生物武器到转基因食物都跟它有关》)。科恩把质粒从细菌中分离出来,在特定的位置切开,插入一段来自不同生物(可以是病毒,或者任何高等动植物,乃至人类)的、带有特定基因的DNA片段,再连结成环状,然后将所得到的重组质粒送回大肠杆菌细胞。随着细菌的生长,细胞中的重组质粒也得到复制扩增——这一过程就叫做基因克隆。质粒就是用来克隆外源基因的载体。任何一种基因通过克隆之后,就可以很容易地在细菌中大量制造出来,供各种研究所用。除了质粒,还有一种感染大肠杆菌的DNA病毒,叫做 λ 噬菌体,也可以作为克隆外源基因的载体。
基因克隆的第一步是取得带有病毒的样品——患非甲非乙型肝炎的病人或黑猩猩的肝脏或血浆,从中分离出核酸,将RNA转化成DNA,与经过切割的 λ 噬菌体载体混合,使之形成重组DNA分子。这样得到的产物叫做基因文库,其中包含大量的重组DNA分子,每个分子带有一个外源基因的插入片段,绝大多数来自病人或者黑猩猩本身的基因组,一小部分可能来自肝炎病毒。
怎样鉴别出那些专属于病毒的基因呢?
霍顿首先尝试分别构建两个基因文库,一个使用肝炎患者的核酸,另一个使用健康个体的核酸,然后通过一些特殊手段,排除两个基因文库共有的基因,只留下肝炎基因文库特有的基因。采用这样的方法,他果然找到了一批只存在于肝炎基因文库的外源基因片段。可是进一步的测试表明,这些都是在感染肝炎病毒后表达量增加的宿主基因产物,代表着宿主对病毒的反应,而不是病毒本身的基因。这个结果表明,实验的思路是正确的,但或许是由于病毒基因的含量太低,所用方法的灵敏度不够,所以失败了。霍顿只能改弦更张,尝试别的办法。
为了提高病毒基因筛选的灵敏度和特异性,减少假阳性结果,在郭劲宏的建议下,霍顿决定采用针对肝炎病毒蛋白质的特异性抗体,但不是用它去直接探测临床样品中的病毒蛋白质,而是间接筛选克隆到噬菌体载体上的病毒基因在细菌里合成的蛋白质产物。
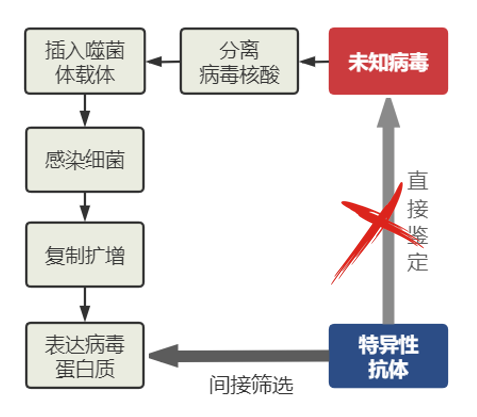
但是,这样的抗体从何而来?唯一可能的来源就是非甲非乙型肝炎病人的血清。
然而,这些血清中究竟有没有霍顿想要的抗体,如果有的话,含量是不是足够,谁也不知道。以乙肝为例,病人血液中有大量的病毒表面抗原,但是却没有针对表面抗原的抗体。只有到了肝炎痊愈,病毒被清除后,这样的抗体才会出现。可是当时却还没有发现罹患非甲非乙型肝炎后自行恢复的病例。
搜寻未知病毒就像是在大海里捕捞一种从来没有人钓到过的鱼。假定在一片海域可能有这种鱼出没,但此鱼的口味十分刁钻,只咬一种从来没人用过、其它鱼类一概不吃的鱼饵。渔夫不知道这个鱼饵是什么,于是就准备了一大批鱼钩和他所能找到的所有的不同食材,每只鱼钩挂上一块,全都扔进海里,然后坐等鱼儿上钩。
采用这样的策略钓鱼能有几分胜算,这是所有人的疑问。但渔夫霍顿还是拿定主意,扬帆出海。为了尽可能提高基因文库中病毒基因的含量,霍顿决定选用一份感染能力最强的非甲非乙型肝炎血液样品来制备基因文库。要做到这一点,多亏了肝炎的黑猩猩模型——将每个待测的病人或者黑猩猩血样逐级稀释,分别接种到黑猩猩体内,观察发病情况,即可找到仍然保持感染能力的最高稀释度。
稀释度越高,表示这份血液中所含的病毒越多。霍顿向CDC的布雷德利要到了一份患病黑猩猩的血浆,其感染能力达到已知的最高水平。他亲自动手,把样品放入离心机高速旋转,使血浆中所含的病毒颗粒沉淀,分离出核酸,制成基因文库,交给朱桂霖。
朱桂霖将基因文库按一定比例与大肠杆菌混合,使其中的一小部分细菌被重组噬菌体感染,然后将细菌平铺在琼脂培养基上。未受感染的细菌在琼脂表面正常生长,连成一片,像草坪一样。进入细胞的噬菌体则开始繁殖复制,同时按照所携带的外源基因片段合成外源蛋白质。噬菌体复制到一定程度后,细菌细胞被杀死破裂,释放出新产生的噬菌体,再感染周围的细菌,开始新一轮的噬菌体DNA复制和外源基因表达。
如此反复循环,最后在长满琼脂表面的不透明的细菌草坪中出现许多透明的斑点,叫做噬菌斑,每个噬菌斑都是因同一个原始重组噬菌体的感染而被杀死的细菌,其中含有扩增后的噬菌体,以及噬菌体所带外源基因的蛋白质产物。只要基因文库与细菌的比例合适,一片直径15厘米的圆形琼脂培养基表面可以有几千个噬菌斑,彼此互不相连。
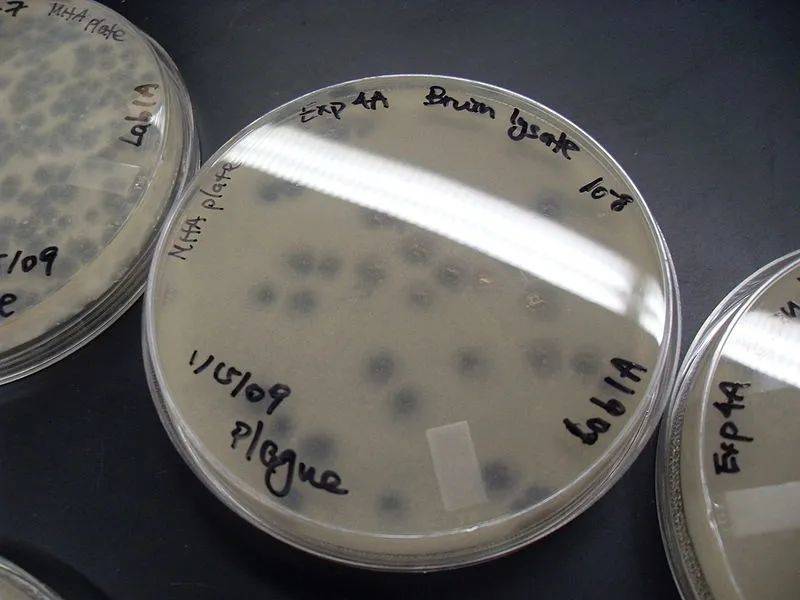
培养基中的白色细菌草坪上的透明圆斑即是病毒制造的噬菌斑丨来源:wikipedia
下一步就是用针对非甲非乙型肝炎病毒蛋白质的抗体,去钓出那些含有病毒蛋白质的噬菌斑,找到病毒基因。霍顿只能寄希望于他用来当鱼饵的肝炎病人血清,希望其中恰好含有这样的抗体。他制作的第一个基因文库经筛选后,没有得到任何病毒基因。于是他另起炉灶,用同一份黑猩猩血液重新制作一个基因文库。这一次在实验过程中不幸发生技术故障,所得到的核酸样品外观不很正常。他犹豫再三,最后决定还是继续进行下去,完成了基因文库的制作,交给同事筛选。
同时,霍顿决定改变抗体的来源,换用一个肝脏炎症特别严重的肝炎病人的血清,理由是症状严重可能是因为病毒复制特别活跃,患者的免疫反应特别强烈,血清中的抗病毒抗体含量也许就特别高。
这一次筛选,总共得到六个阳性的噬菌斑,从中分离出六个重组噬菌体。其中是不是带有病毒基因?由于早先的技术故障,所有人都不抱多少希望。后续的测试不出所料地将这六个克隆的基因一个接一个地排除……轮到最后一个克隆基因了,实验记录本上的编号是5-1-1,竟然并非来源于黑猩猩宿主的基因组,而是一个前所未知的基因,极有可能就是新病毒!
随后的6个月里进行的一系列测试终于没有令人失望。5-1-1号克隆的确来自一种新病毒的RNA,但只是它的一小段。这一点难不倒研究人员。他们很快就以这个小片段作为把手,从基因文库中把与它重叠的新病毒RNA片段逐一找到,拼接成完整的病毒RNA,发现5-1-1号克隆只占它的1.5%。霍顿将新病毒正式命名为丙型肝炎病毒[7]。
值得一提的是,得到5-1-1号克隆以后,霍顿又用同一份黑猩猩血液制作了几个基因文库,却再也没有直接筛选到来自同一病毒的第二个克隆,充分说明了这条技术路线的困难程度。在不得已的情况下采取一个近乎赌博的全新策略,居然能如愿以偿地找到未知的新病毒,不能说不包含几分运气的成分。可是机遇只会眷顾永不放弃的追求者。霍顿成功的背后是整个团队连续六年坚持不懈的努力,数不清的失败,以及累计筛选数以千万计的重组噬菌体的巨大工作量。
霍顿的工作之所以意义重大,不仅在于他发现了一个临床医学上十分重要的新病毒,还在于他开创了一条搜寻未知病原体的全新途径,启迪了其他新的病原体的发现,堪称居功至伟。
霍顿团队通过这条途径发现丙肝病毒的过程之所以如此曲折艰难,主要的障碍就是丙肝病毒的遗传物质及其基因产物在血液中的含量比其它一些病毒,例如乙肝病毒,低得多。要到以PCR为基础的核酸扩增技术开发完善并普遍应用之后,这个障碍才被逐步克服。新一代核酸测序技术以及生物信息学的发展,更大大加快了病原体的发现和鉴定过程。时至今日,对于一种未知的新发病原体,例如新冠病毒,从采集样品到测定病毒基因序列并确定其为新型病毒,很可能只需要短短几天[8]。三十年来分子生物学飞速发展,带来的变化何止天翻地覆!
发现丙型肝炎病毒以后,霍顿团队当即利用基因工程的方法,将病毒基因转移到大肠杆菌和酵母菌中,制造出病毒蛋白质,作为抗原,来检测血液中是否存在针对它们的抗体。他们发现,这样的抗体只存在于患有丙型肝炎(即非甲非乙型肝炎)的黑猩猩血清中,而不在患有甲型或乙型肝炎的黑猩猩血中。这表明,这样制造出来的病毒蛋白质可以作为丙型肝炎的诊断试剂!
于是,霍顿向阿尔特索取了他的那套标准血清样品,用来进行最后的评判。所有的非甲非乙型肝炎样品都测出阳性结果,无一漏网;所有的对照样品都测出阴性结果,明白无误。试验圆满成功,阿尔特梦寐以求的丙型肝炎诊断试剂终于诞生了[9]。
1990年,凯荣公司的丙型肝炎诊断试剂被FDA正式批准,并用于为美国所有的血库筛选供血者。到了1992年,美国输血后肝炎的发病率降到了1.5%。此后,丙型肝炎诊断试剂又得到改进,检测灵敏度进一步提高。从1992年到1997年,阿尔特跟踪研究了650例接受输血的病人,没有发现一例输血后肝炎,发病率降到了0.15%以下,与1970年相比,降幅高达200倍。
为什么发病率没有完全降到零?一般认为,这并不是由于血液中还存在未知的肝炎病毒,而是因为肝炎病毒感染人体后,要经过一段时间才能产生抗体,而在这段空窗期内,血液里的病毒已经能够传染肝炎。采用以PCR为基础的高灵敏度核酸扩增方法来直接探测丙肝病毒RNA,就可以解决这个残留的输血安全问题。
阿尔特和霍顿对防止输血后肝炎和发现丙肝病毒做出了杰出的贡献,2000年,二人荣获被视为诺奖风向标的拉斯克临床医学奖。
1957年,英国病毒学家艾萨克斯(Alick Isaacs)和林登曼(Jean Lindenmann)正在研究流感病毒。当时已知流感病毒能感染体外培养的鸡胚胎细胞,把细胞杀死。不过二人发现,如果先用加热灭活的流感病毒处理细胞,细胞就能对流感病毒产生抵抗力,之后再遇到活病毒,也不会被感染。他们推测,鸡胚细胞接触到死的流感病毒以后能产生某种物质,抑制流感病毒的生长。他们把这种物质命名为“干扰素”。
保护我们身体的免疫大军中有一支前哨部队,称为天然免疫系统,它是人体与生俱来的保护机制,构成对抗病原体感染的第一道防线。这支前哨部队的一个主要武器,是由人体细胞产生的具有不同免疫功能的一些小分子蛋白质,统称为细胞因子。干扰素就是一类重要的细胞因子。继艾萨克斯和林登曼之后,其他研究者陆续发现干扰素有许多重要的功能,例如直接抑制病毒的复制繁殖。而且干扰素的抗病毒作用没有专一性,并非只针对流感病毒,而是对许多病毒都有效。
早在丙肝病毒发现之前的1986年,就有人尝试用干扰素治疗非甲非乙型肝炎,并且取得了不错的效果。1991年,干扰素被正式批准用于治疗丙肝。以干扰素配合一种小分子抗病毒药利巴韦林(ribavirin),用于丙型肝炎,可以在大约一半的病人中实现清除病毒,彻底治愈的理想效果。由此,丙肝成为干扰素在临床应用中最主要的适应症。
遗憾的是,干扰素疗法的副作用极为严重。接受治疗的病人会出现发热、疲倦、肌肉酸痛等等一系列症状,类似得了流感。这是因为人体被流感病毒感染后,天然免疫系统受病毒刺激,产生干扰素来对抗感染。流感的临床症状,在很大程度上属于体内产生的干扰素及其它细胞因子的副作用。除此之外,干扰素还可能引起严重的抑郁症。许多病人由于不能忍受这些副作用,无法完成24周到48周的正常疗程,被迫降低剂量或者中断治疗,严重影响了疗效。
治疗丙肝的高效低毒的理想药物,直到2010年才出现。这一里程碑式的重大进展,可以追溯到丙肝病毒发现伊始的1990年代。其中的两位关键人物,在他们开始进行研究时,未必预见到自己的工作日后会有如此深远的影响。
尽管霍顿得到的丙肝病毒基因克隆为开发丙肝检测试剂铺平了道路,但要证明这一新病毒的确是非甲非乙型肝炎的病原体, 还缺少最后一个关键证据,那就是将克隆的病毒基因组接种到黑猩猩中,能引起非甲非乙型肝炎。
除此之外,为了研究丙肝病毒的生物学性状,尤其是在肝细胞中复制生长的特性,就必须让病毒在实验室里培养的细胞中生长。丙肝病毒基因组被克隆以后,就有人将它输入体外培养的细胞中,结果发现,虽然克隆的病毒基因组可以指导合成病毒的各种蛋白质,却不能产生新的病毒颗粒。原因何在?
1996年,美国圣路易斯华盛顿大学的病毒学家莱斯(Charles Rice)发现,丙肝病毒RNA分子的末端有个特别的结构,在被克隆的丙肝病毒基因组中丢失了。会不会就是这个缺失的结构影响了病毒的生长复制?
莱斯构建了新的丙肝病毒基因组克隆,将RNA分子末端的这个结构添补回去,然后满怀希望地把这个“完整”的病毒RNA注射到黑猩猩肝脏内。黑猩猩还是没有得上肝炎,哪怕表现出任何遭到感染的迹象。实验失败了。
不为挫折所阻,莱斯继续探索。他进一步发现,克隆得到的丙肝病毒基因组中有一些突变。他推测,这些突变可能在被克隆之前就已存在于宿主内,也可能是在被人工克隆的过程中发生的。不论是哪一种情况,突变可能影响了病毒RNA的复制能力。那么怎样才能把这些突变恢复到突变发生前的核苷酸呢?
突变发生的位点是随机的,不同的RNA分子可能在不同的位点存在突变。莱斯分析比较了一大批克隆得到的病毒RNA分子,找到每一个存在变异的位点,在这个位点上选用最普遍的公用核苷酸来尝试修正突变造成的变异。用这样的方法,莱斯构建出丙肝病毒的一个“共有基因序列”,把它注射到黑猩猩体内,果然引起了肝炎!这表明,他已经得到了一个具有感染能力的丙肝病毒基因组[10]。这一重要突破不仅坐实了丙肝病毒就是非甲非乙型肝炎的病原体,而且为丙肝病毒的分子生物学研究奠定了基础。
2001年,莱斯离开华盛顿大学,加盟纽约的洛克菲勒大学。洛克菲勒大学是美国历史悠久的病毒学研究摇篮,曾经孕育了包括流感病毒、黄热病毒、脊灰病毒等一系列重要病原体的许多重大发现。莱斯的到来又使之成为丙肝病毒的研究重镇,取得一系列开创性的成果。
大约与莱斯同时,德国美茵茨大学的病毒学家巴腾许拉格(Ralf Bartenschlager)也构建了一个丙肝病毒的共有基因序列。他想让这个病毒基因组在体外培养的肝脏细胞中复制生长,却失败了。改用莱斯的克隆以后,还是没有成功。
巴腾许拉格后来转到德国最古老的海德堡大学任教,在风光旖旎的内卡河畔继续探索这个难题。他联想到与丙肝病毒有亲缘关系的其它一些病毒,基因组中即使丢失了某些基因,病毒RNA还能在细胞中复制。如果去掉丙肝病毒基因组中那些与RNA复制无直接关系的部分,例如编码病毒外壳蛋白质的那些基因,只留下RNA复制所必须的部分,让病毒丢掉包袱,轻装上路,是不是就能提高病毒RNA在培养细胞中的复制效率?像这样精简而成的人造病毒结构叫做“复制子”。这一次,试验终于成功了[11]!
随后,巴腾许拉格与莱斯对复制子系统的病毒RNA以及细胞株进行了一系列改进,终于得到了可以在培养细胞中高效复制的丙肝病毒RNA。虽然复制子不带病毒的外壳蛋白质基因,不能包装出完整的病毒颗粒,但可以用来研究丙肝病毒RNA复制的生物学机制。更重要的是,它有可能用来在体外高效快速地筛选抑制丙肝病毒复制的化合物分子,作为治疗丙肝的候选药物。
在此之前,有效的小分子抗病毒药物寥寥无几。由美国政府资助的生物医学类研究课题中,有关艾滋病的研究在资助金额上多年独占鳌头,取得的成果是由几种抗HIV药物联合组成的高效抗逆转录病毒疗法 (HAART),即所谓的“鸡尾酒疗法”。 它可以有效地延长患者生命,却无法将病毒彻底清除,充分说明了开发抗病毒药物的艰难程度(参阅《鸡尾酒疗法问世与南非艾滋悲剧——谁之功,谁之过?| “世纪绝症”的四十年(下)》)。尽管如此,在丙肝病毒复制子系统问世以后,还是有一批研究人员投入了海选抗丙肝化学药物的比拼,竞争极为激烈。
丙肝病毒RNA的复制依靠的是蛋白质NS5B,即病毒本身的RNA聚合酶。复制所用的原料分子是核苷酸,根据病毒的单链RNA分子的核苷酸序列,RNA聚合酶将原料核苷酸一一连结起来,形成新的病毒RNA。丙肝病毒有许多不同的基因型,彼此之间差异很大,但是这些不同基因型的RNA聚合酶则十分相似,这意味着,只要找到一种能抑制RNA聚合酶活性的药物,就可能对各种基因型的病毒都有效,起到事半功倍的效果。
美国新泽西州有一家研制抗病毒药物的小公司,叫做法莫赛特(Pharmasset),利用丙肝复制子系统找到一些化学结构类似于核苷酸的小分子化合物。这些核苷酸类似物能被丙肝病毒的RNA聚合酶误认为是制造RNA的核苷酸原料,添加到新合成的RNA链上;可是这些伪装的原料分子一旦进入位置,下一个核苷酸就再也连接不上,病毒RNA的延长就此终止。
看来这些核苷酸类似物有希望成为抑制丙肝病毒RNA复制的药物。可是,这些化合物到了动物体内后,就都出了问题,有些很快就降解失效,有些难以进入肝细胞,研究就此停滞不前。
2005年,法莫赛特公司延聘刚离开一家大药厂的化学家索非亚(Michael Sofia),负责抗丙肝病毒药物的研制,希望他能将这一项目带出困境。索非亚与他的团队成员殚精竭虑,尝试对那些核苷酸类似物的化学结构进行各种各样的修改。他们发现,进入细胞的核苷酸类似物本身的抗病毒能力并不强,可是经过细胞内所含一系列代谢酶的作用,能够转化成为具有高活性的分子结构,有效抑制病毒RNA的复制。但原有的核苷酸类似物接受这种转化的效率很低,必须改用另一种结构略有不同的前体。
可是那种前体分子又带有负电荷,无法穿过肝细胞表面的细胞膜。为了使它能穿膜进入肝细胞,又必须设法作进一步的修饰,将负电荷屏蔽起来……就这样,每一个问题的解决,总是伴随着新问题的产生。成功的希望,一次又一次地被打碎,最后目标似乎总是可望而不可及。
索非亚早年在康奈尔大学求学,曾以本科生的身份到一个化学教授的实验室当助手。他开始做第一个实验时,有个研究生学长将他拉到一旁,郑重其事地告诫:“你得明白,来做研究,你的努力只有百分之二十能成功,百分之八十全是失败。所以你得满足于百分之二十的成功率。要不然,就趁早别干。” 多年以后,索非亚谈到研制丙肝药物的个中艰辛时,回忆起那位师兄,说道:“现在我终于晓得,他可真是个乐天派啊!”
经历了无数次的失败,索非亚与他的团队终于成功设计出一个不带电荷的药物分子,可以顺利地进入肝细胞内,经由肝细胞内特有的一种代谢酶的作用,脱去屏蔽,暴露出负电荷,成为活性物质的前体。由于带有负电荷,这些前体分子无法再穿过细胞膜离开肝细胞,只能在肝细胞内逐步转变成抑制病毒RNA复制的活性结构。
同时,人体内的其它细胞不含有那种特殊的酶,不会留存药物分子,这就大大降低了药物对人体的毒副作用。所有研究人员孜孜以求的口服高效低毒抗丙肝药物终于诞生了,起名为索非布韦(sofosbuvir)[12]。当索非亚在一个专业会议上首次披露这一成果时,全场鸦雀无声。盯着屏幕上显示的数据,另一家公司的一个与会者喃喃地自言自语:“比赛结束了……”
2012年,美国研制抗病毒药物的龙头老大吉利德(Gilead)公司以112亿美元的高价收购了法莫赛特。2013年,美国FDA正式批准索非布韦用于治疗慢性丙型肝炎,吉利德公司随即将它推向市场。除了索非布韦,还有另一种药物雷迪帕韦(ledipasvir)同样是经由复制子系统筛选得到,但针对的靶标是丙肝病毒的另一种蛋白质NS5A。这两种药物联用,只需经过8至12周的治疗,94%至99%的病人都能清除病毒,彻底痊愈,而且副作用极低。
丙肝治疗特效药的诞生过程充分说明,成功的转化医学研究和药物开发离不开坚实的基础研究。研制抗丙肝病毒药的巨大成功,为人类消除丙型肝炎带来了曙光。2016年,世卫组织(WHO)制定了预防和治疗双管齐下,到2030年在全球基本控制乙型肝炎和丙型肝炎的规划。
对于丙型肝炎来说,由于缺少有效的疫苗,实现这一目标的关键在于广泛开展病毒核酸检测,找到慢性患者,特别是无症状病毒携带者,积极进行抗病毒治疗。一个没有丙型肝炎的新世界已经出现在地平线上。这一美好愿景的实现,将为丙肝研究人员近半个世纪的艰苦努力树立一座丰碑。这一群体的三位杰出代表——阿尔特、霍顿和莱斯——荣获2020年的诺贝尔生理学或医学奖,自是实至名归;然而每一奖项每年最多三人获奖的规定,难免造成遗珠之憾。
在此之前的2016年,巴腾许拉格、莱斯和索非亚由于对丙肝病毒体外复制系统及治疗药物作出了杰出贡献,共同获得拉斯克临床医学奖。颁奖仪式上,莱斯分享了他认识的一个家庭的故事。二十年前,这家一个幼小的女儿不幸感染了丙型肝炎。夫妇二人不知是否应让爱女接受副作用严重且疗效不确定的干扰素治疗。痛苦纠结之中,他们找到莱斯,征询意见。
最后夫妇二人决定暂缓治疗,等待新疗法的问世。就在拉斯克奖颁奖仪式的前一周,这对夫妻来信祝贺莱斯获奖,同时向他报喜:他们的女儿经过新一代抗丙肝药物的治疗,已经痊愈,结婚,家庭幸福,有了个一岁半的女儿,而且正怀着第二胎。“作为一个从事基础研究的科学家,没有一项褒奖比这更大,来得更出人意料。”莱斯动情地说。
莱斯的真情表露,代表了广大丙肝病毒研究人员的心声。
主要参考资料:
1. Houghton M. The long and winding road leading to the identification of the hepatitis C virus. J Hepatol. 2009; 51: 939-48.
2. 2000 Lasker Clinical Medical Research Award. http://www.laskerfoundation.org/awards/show/hepatitis-c-virus-and-its-detection-in-blood-for-transfusions/.
3. 2016 Lasker Clinical Medical Research Award. http://www.laskerfoundation.org/awards/show/hepatitis-c-replicon-system-and-drug-development/.
其他参考文献:
[1] WHO. Hepatitis C. 2020. https://www.who.int/news-room/fact-sheets/detail/hepatitis-c.
[2] Gao Y et al. 2019 https://doi.org/10.1093/ofid/ofz040.
[3] Alter HJ et al. Hepatitis-associated antigen. To test or not to test? Lancet. 1970; 2: 142-3.
[4] Alter HJ et al. Posttransfusion hepatitis after exclusion of commercial and hepatitis-B antigen-positive donors. Ann Intern Med. 1972; 77: 691-9.
[5] Feinstone SM et al. Transfusion-associated hepatitis not due to viral hepatitis type A or B. N Engl J Med. 1975; 292: 767-70.
[6] Alter HJ et al. Transmissible agent in non-A, non-B hepatitis. Lancet. 1978; 1: 459-63.
[7] Choo QL et al. Isolation of a cDNA clone derived from a blood-borne non-A, non-B viral hepatitis genome. Science. 1989; 244: 359-62.
[8] Ren LL et al. Identification of a novel coronavirus causing severe pneumonia in human: a descriptive study. Chin Med J (Engl). 2020; 133: 1015‐24.
[9] Kuo G et al. An assay for circulating antibodies to a major etiologic virus of human non-A, non-B hepatitis. Science. 1989; 244:362-364.
[10] Kolykhalov AA et al. Transmission of hepatitis C by intrahepatic inoculation with transcribed RNA. Science. 1997; 277: 570-4.
[11] Lohmann V et al. Replication of subgenomic hepatitis C virus RNAs in a hepatoma cell line. Science. 1999; 285: 110–13.
[12] Sofia MJ et al. Discovery of a β-d-2'-deoxy-2'-α-fluoro-2'-β-C-methyluridine nucleotide prodrug (PSI-7977) for the treatment of hepatitis C virus. J Med Chem. 2010; 53: 7202-18.
本文来自微信公众号:返朴(ID:fanpu2019),作者:何笑松(加州大学戴维斯医学院退休教授)