
扫码打开虎嗅APP

本文来自微信公众号: RNAScript ,作者:一一
前言
2025年5月,一名患有氨甲酰磷酸合成酶1缺乏症的新生儿接受了全球首例个体化碱基编辑治疗,递送载体是脂质纳米颗粒(LNP)。一个月后,Elevidys相关安全性事件持续发酵:这款AAV基因疗法因患者死亡事件被推至监管审查中心,相关临床研究也被按下暂停键。与此同时,细胞外囊泡(EV)相关基因递送候选物仍在临床早期艰难推进,多项I期试验还在回答安全性、有效性与CMC可控性这些基础问题。
三个平台,在同一个时间窗口里,同时呈现出突破、危机与不确定性并存的状态。
近日,得克萨斯大学安德森癌症中心Betty Y.S.Kim、姜文、北京大学深圳研究生院Andrew S.Lee等人于《Nature Biomedical Engineering》上发表了一篇系统综述“Engineering challenges and translational opportunities in emerging gene delivery platforms”,对AAV、LNP和EV这三大基因递送平台进行了迄今最全面的横向比较,廓清了每个平台真实的边界与局限。
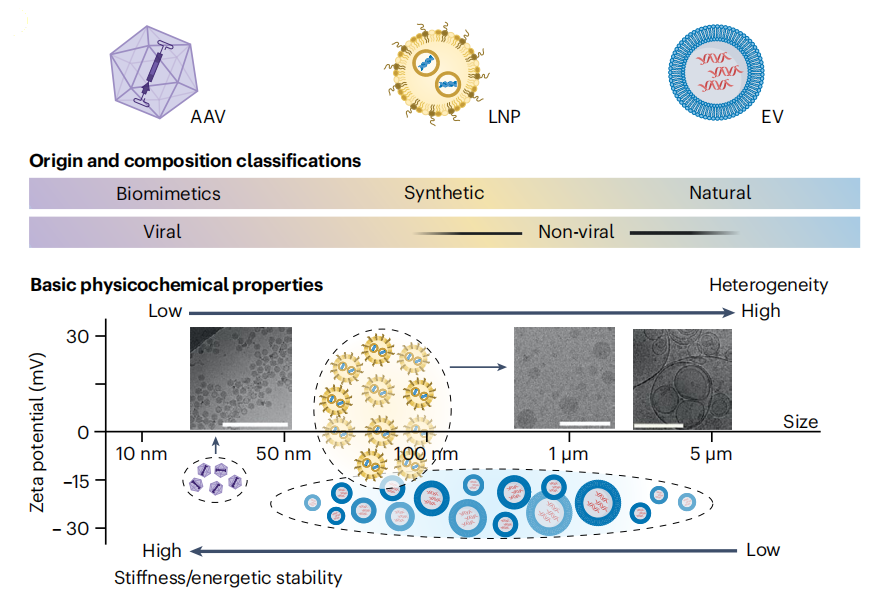
如果把AAV、LNP和EV放在同一张表里比较,会发现它们并不是沿着同一条赛道在竞争,而是在三组根本变量上形成错位:能装什么、能到哪里、进去以后能不能真正表达。
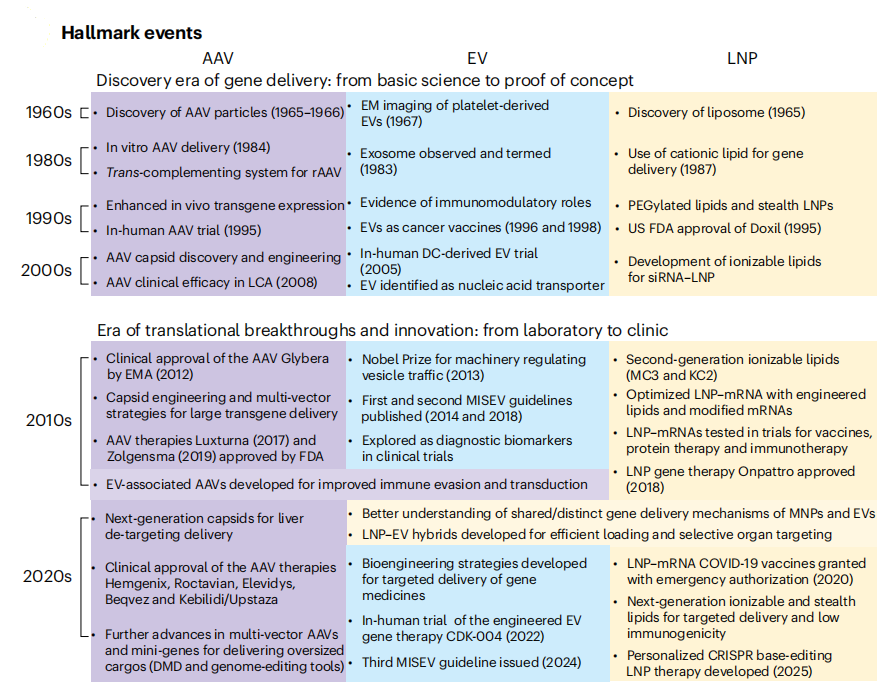
货物兼容性,平台选择最底层的约束
AAV的载量天花板清晰:约4.7 kb的单链DNA,直接把DMD全长基因、碱基编辑器、先导编辑器挡在门外。双载体系统、迷你基因等补救方案一直在优化,但普遍承认的代价是转导效率下滑、生产成本上升,以及异常转基因产物风险的增加。
LNP则几乎没有严格的尺寸天花板。临床优化的LNP对1–5 kb mRNA的封装效率超过90%,自扩增RNA(saRNA,9–12 kb)也能达到70%–90%。这种灵活性,是LNP在COVID-19疫苗之后持续拓宽应用边界的底层逻辑。
EV的问题不在尺寸,而在装载效率。天然EV主要携带小型非编码RNA,对全长mRNA的装载量极低——每个囊泡大约1–10个拷贝,即使辅以电穿孔,封装效率也很少超过30%,与LNP形成数量级的落差。这个数字从根本上限制了EV在mRNA系统性递送中的可行性,也解释了为什么当前EV临床试验仍集中在较窄适应症。
LNP进入细胞后,大多数颗粒被运送至溶酶体降解,内体逃逸比例仅约1%–2%。这意味着,即使LNP高效完成了mRNA封装,绝大多数货物在到达核糖体之前就已失活。
EV在这一步呈现出内在优势:通过磷脂酰丝氨酸和四跨膜蛋白介导的膜融合,其内体逃逸率约为20%,显著高于LNP。一项胰腺癌模型的对比研究显示,EV的溶酶体滞留率为5.7%,LNP为26%;在仅使用LNP十分之一RNA剂量的条件下,EV实现了更强的肿瘤抑制和更长的生存期。吸入给药场景中,EV递送IL-12 mRNA的蛋白表达量约为脂质体的2.2倍。
但这组数据必须放回完整的上下文来理解:EV的高逃逸率建立在极低装载量的基础上,而LNP即便逃逸效率低下,凭借远胜于EV的货物数量,在蛋白表达总量上仍能维持竞争力。人促红细胞生成素mRNA的对照实验显示,等剂量RNA条件下,MC3-LNP的表达量比EV高出6–8倍。两个指标必须放在一起看,彼此不可孤立。
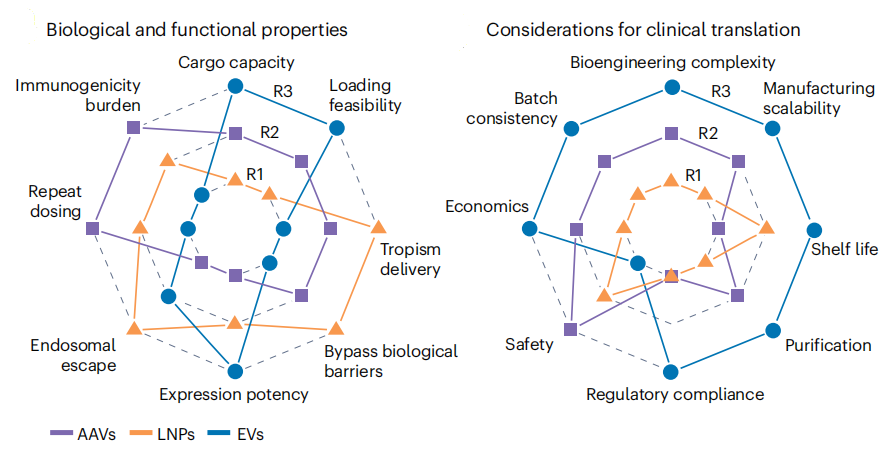
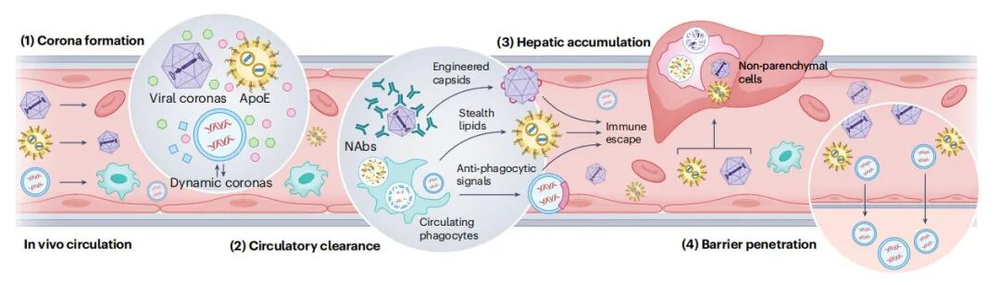
AAV在人群中的预存免疫问题相当突出:AAV1/2的血清阳性率达60%–80%,直接影响转导效率并将大量患者排除在外。高剂量全身给药可诱发T细胞介导的肝毒性和补体驱动的微血管病变,Elevidys相关安全性事件再次将这一隐患推至前台。
LNP在COVID-19疫苗时代建立了良好的安全性记录,但并非毫无隐忧。PEG化脂质可能诱发抗PEG抗体,限制重复给药次数;体外转录mRNA及saRNA中残留的双链RNA副产物可激活天然免疫通路。TLR7/8的激活在疫苗场景中可以被接受,在基因编辑或再生医学中则可能构成更棘手的问题。得益于核苷修饰和严格的dsRNA去除工艺,这类风险在已获批的疫苗和部分RNA药物中已显著降低;但在基因编辑、再生医学或高频重复给药等场景中,免疫激活仍然是需要单独评估和谨慎应对的问题。
EV的低免疫原性植根于其内源性起源,在理念上最贴近生物相容性的理想。一项对比研究显示,EV递送I型胶原α1 mRNA引发的局部炎症显著低于MC3-LNP;VEGF-A递送实验中,EV引发的细胞因子释放和免疫激活也是三者中最少的。但EV的免疫原性高度依赖于供体细胞来源、纯化方法和工程化改造步骤,目前能支撑系统性判断的数据仍相当有限。
LNP的临床成熟度在三个平台中无可争议地最高。Onpattro于2018年获批,COVID-19 mRNA疫苗的全球规模化部署则充分验证了这一体系的生产可扩展性。而近年来最引人注目的数据来自体内基因编辑领域:
NTLA-2001单次静脉输注后,转甲状腺素蛋白降幅达96%;NTLA-2002在遗传性血管性水肿患者中实现超过85%的蛋白敲降,几乎所有患者达到无发作状态;CD117-LNP递送腺嘌呤碱基编辑器修正镰状细胞病β-珠蛋白突变,在长期重建细胞中实现了48%的编辑效率。这些数字标志着LNP正从mRNA递送工具,向基因编辑核心载体完成一次实质性的身份跃迁。
然而,肝外递送仍是系统性的短板。静脉注射后,约90%的LNP在1小时内被肝脏摄取。选择性器官靶向技术通过调整脂质组分改变器官分布,已在肺、脾等器官取得临床前验证,但临床数据的积累远不及肝脏靶向那样深厚。内体逃逸1%–2%的效率天花板,也难以单靠配方微调来根本突破。新一代可离子化脂质、pH响应性融合肽以及proton sponge类添加剂的组合策略正在推进,近期一种基于正高斯曲率fusogenic cubosomes的方法,实现了10分钟内接近100%的mRNA装载和更高效的膜融合——这个方向,很可能构成LNP工程化的下一个关键节点。
EV在穿越生物屏障方面展现出了独特能力:对血脑屏障的穿透力、天然的低免疫原性、内在的组织归巢倾向——这些特质让EV在中枢神经系统疾病、肺部疾病和眼科疾病等“难以抵达”的适应症中,拥有真实而鲜活的差异化价值。
一项对比研究显示,双靶向EV在胰腺癌模型中的肿瘤积聚量达到LNP的2–3倍。心脏祖细胞来源的EV经肌肉注射后,心脏局部mRNA递送比例达56%,而LNP仅为19%。
但EV的临床转化仍被两个未系统解决的问题拖住脚步。其一是生产的均一性和可扩展性:EV的天然异质性使批次间一致性极难保证,GMP级别纯化方法在产率和纯度之间的取舍至今没有统一答案,现有方法的产率波动在5%到60%之间。其二是监管路径的模糊:目前尚无专门针对EV基因疗法的监管框架,天然EV、工程化EV和负载外源货物的EV在监管分类上仍存在歧义。综述中提到,Capricor Therapeutics的CAP-1002——一种心球来源、具有EV富集属性的DMD治疗候选物——因有效性不足和CMC问题遭FDA拒绝,成为EV类疗法临床转化不确定性的典型案例之一。
这篇综述中最具产业参考价值的部分,是对跨平台杂合策略的分析。
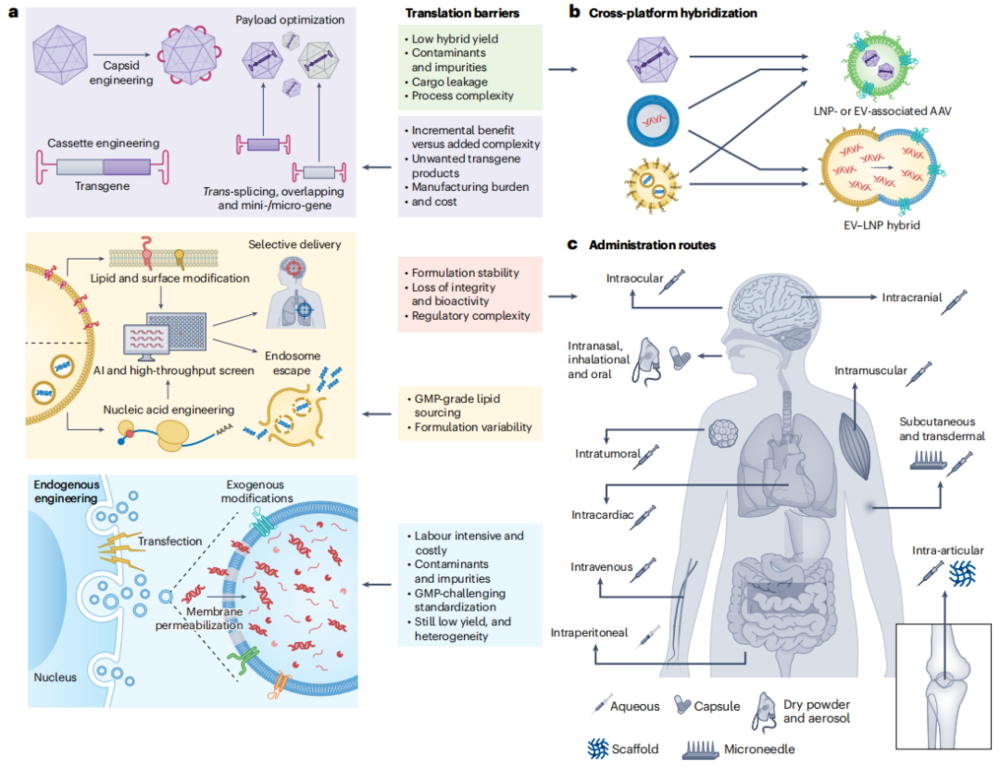
LNP或EV包裹AAV的杂合策略,通过脂质膜遮蔽衣壳表位,降低中和抗体识别率,提高血清稳定性。EV-AAV6/9构建体在免疫动物模型中的心脏转导效率达到单独AAV的两倍以上,肺部模型同样观察到明显改善。这类杂合体的工程化难点在于共包装效率偏低——传统AAV生产方式对EV相关AAV的富集效率不足20%,还需额外引入分离纯化步骤。
EV-LNP杂合策略尝试将LNP的高载量能力与EV的天然靶向性和低免疫原性黏合在一起,多通过冻融、超声、挤出、PEG等手段诱导膜融合实现组装。核心挑战在于融合过程中的货物泄漏和粒子聚集。前述fusogenic cubosomes方法代表了这一方向迄今最具吸引力的推进。
杂合策略背后有一个朴素的思路:没有一个平台是万能的,将各平台的互补优势组装到一起,可能比在单一平台上进行极限工程优化来得更有效。
这篇综述在结论部分点出了一个不容回避的现实:关于三个平台的头对头比较研究至今极度匮乏。已有的对比研究中,不少存在控制变量不等效的问题——剂量不匹配、配方优化程度不对等——使得结论的可推广性打了折扣。
这个判断并不仅仅关乎学术圈的自我要求。对于研发端而言,当“应该选LNP还是EV”这样的决策无法得到标准化头对头数据的支撑,选择就很难不受到先入为主的平台偏好的影响。
另一个被综述特意拎出来的维度是患者个体差异:年龄、性别、代谢状态和免疫状态都会显著影响LNP的生物分布和表达水平,但现有临床研究对这些因素的系统记录远远不够。年龄对LNP吞噬清除效率的影响已有直接证据,性别差异对纳米医学效能的扰动也有初步数据显露端倪。这些变量不是背景噪声,而是决定疗法在真实人群中能否起效的关键参数。
基因递送的平台之争,说到底,是不同工程哲学之间的博弈:AAV依赖生物识别的精确性,LNP信奉化学成分的可调性,EV追求内源仿生的兼容性。三者都有不容忽视的临床价值,也都有尚未触及根基的核心局限。在一个碱基编辑器已经走进新生儿病房、CAR-T体内编程正在开启首批临床试验的时代,递送平台的选择,将直接决定哪些疾病能够率先走到患者面前。