
扫码打开虎嗅APP

本文来自微信公众号:奇点网(ID:geekheal_com),作者:张艾迪,原文标题:《《科学》:饭吃八分饱,免疫不怕老!重新解读迄今最大队列研究,发现长期热量摄入减少14%可逆转胸腺衰老,并找到新抗衰关键因子》,头图来自:unsplash
家人们,吃饭少吃点儿不仅能给钱包续命,还能给免疫功能续命!
近日,来自美国耶鲁大学的Vishwa Deep Dixit和他的同事们,基于迄今最大人类热量限制队列研究CALERIE的数据,于《科学》上发表重磅研究成果,为热量限制能够延长健康寿命、延缓衰老再添力证[1]。
在对218名健康人长达2年的随访数据进行分析后,研究者们提出,长期热量摄入减少14%能够使重要免疫器官——胸腺恢复活力,增加胸腺产生T细胞的能力,从而改善免疫功能随年龄增长而衰退的现象。
另外,他们还挖到了新抗衰关键因子——Pla2g7。Pla2g7基因表达缺失与热量限制的效果差不多,不仅也能给胸腺续命,还能有效改善脂肪代谢、与年龄相关的炎症反应等问题。

论文首页截图
如今,热量限制饮食和健康延寿之间似乎已经划上了等号。出于对健康长寿的本能追求,再加上吃吃吃的基本生存需求,人们从来没有放弃探索热量限制的秘密。
大量实验室动物的基础研究表明,限制果蝇、小鼠、线虫、甚至是非人类灵长动物的热量摄入,长期控制其卡路里摄入量减少40%,即可以延长这些动物在实验室条件下的健康寿命[1]。
那么,对于我们人类来说,在保证安全性的前提下,热量限制能给健康寿命带来多少益处呢?
科学家们也不断试图从人类队列研究中追求真相,其中,CALERIE研究不仅是首个热量限制随机对照队列研究,也是迄今为止最大的相关队列研究。
CALERIE研究共招募218名年龄在21岁~50岁的健康人,体重指数(BMI)在22–28.0kg/m2之间。他们随机按2:1分为热量限制组和对照组,对照组参与者照常吃喝,热量限制组的参与者则要求每天热量摄入减少25%(≈实验室动物热量摄入减少40%)[2]。
然而,这项试验中出了点儿小插曲——参与者们真的很难管住自己的嘴啊!实际上,热量限制组的参与者热量摄入只降低了14%。
虽然和设想有些出入,但科学家们表示这并不碍事。
一些基于CALERIE数据的分析结果表明,一方面,这种8.5分饱的热量限制并不会影响到参与者的情绪、生活质量、睡眠和性功能等健康问题[3];另一方面,热量限制明显改善了参与者们健康状况,如减少脂肪、改善胰岛素敏感性、降低心血管疾病的风险标志物水平等[2-5]。
就这么说吧,CALERIE队列阴差阳错地证明,坚持2年吃饭控制在8.5分饱就能给健康寿命带来很大收益,也不会饿出啥毛病。

这次,耶鲁大学的学者们决定再次挖掘CALERIE研究的价值,让免疫器官——胸腺来告诉我们,热量限制究竟给我们的机体功能带来哪些改变。
要知道,人体免疫功能衰退的一个重要特征就是,胸腺失去大量生成T细胞的能力。可随着年龄增长,胸腺会比其它器官更早衰老,表现为胸腺脂质积累增加、T细胞产量减少,等到50岁时,大约80%的胸腺被脂肪组织所替代[6]。
一旦胸腺“退休”不再大量产生新的T细胞,当新的病原体入侵机体时,剩下的T细胞也是束手无策。这也就是为何说老人抵抗力较弱。
而在对比两组参与者在基线和随访第2年时的胸腺功能变化后,研究者们发现,热量限制竟能让胸腺“返老还童”。
热量限制组的参与者胸腺体积显著增加;且在相关转录组没有受到影响的情况下,新生CD4+T细胞和新生CD8+T细胞数量也都明显增多。反观对照组的参与者,他们的胸腺体积、功能在这两年期间并没有发生显著变化。
也就是说,热量限制能够挽救T细胞生产力,给免疫功能续上一大口命!
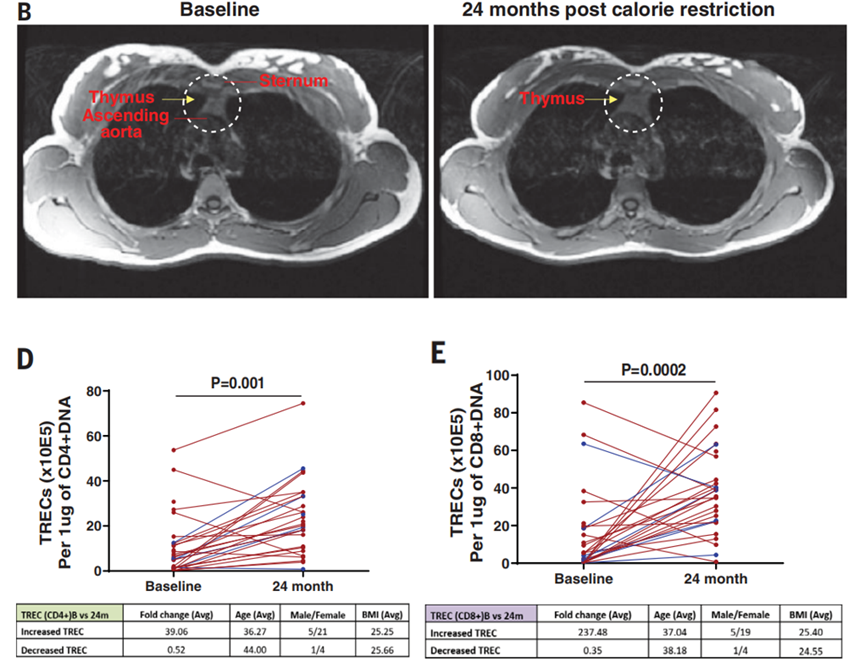
热量限制推迟了胸腺的退休年龄
除此之外,研究者们在对参与者腹部脂肪组织中的基因表达谱进行识别后,还找到了热量限制导致脂肪组织重构的证据,发现代谢、先天免疫以及炎症途径中的相关基因(Sparc,Plin5,Acvr1c,Pde3a,Nampt,Ppara等)表达发生上调或下调。
其中,因热量限制而表达明显下调的Pla2g7基因引起了研究者们的注意。
Pla2g7基因编码的蛋白PLA2G7由巨噬细胞分泌,可以降解血小板活化因子,是炎症的强效激活剂,与脂质代谢有关。在临床研究中, 血液中较高PLA2G7水平与许多代谢、免疫功能障碍的疾病有关,例如中风、慢性阻塞性肺疾病、自身免疫性疾病、心血管疾病、2型糖尿病等[7]。
这么看来,PLA2G7蛋白真是出现在各大犯罪现场。于是研究者们决定进一步查明PLA2G7蛋白在此处的作用。
他们将小鼠的Pla2g7基因敲除,并与野生型小鼠进行对比。结果发现,Pla2g7基因表达缺失几乎完全复制了热量限制的效果。
一方面,Pla2g7基因表达缺失减轻了小鼠与年龄相关的炎症,并改善其代谢能力,比如增加脂肪组织脂解、减少肝脏脂肪变性、降低循环中促炎性细胞因子水平等。
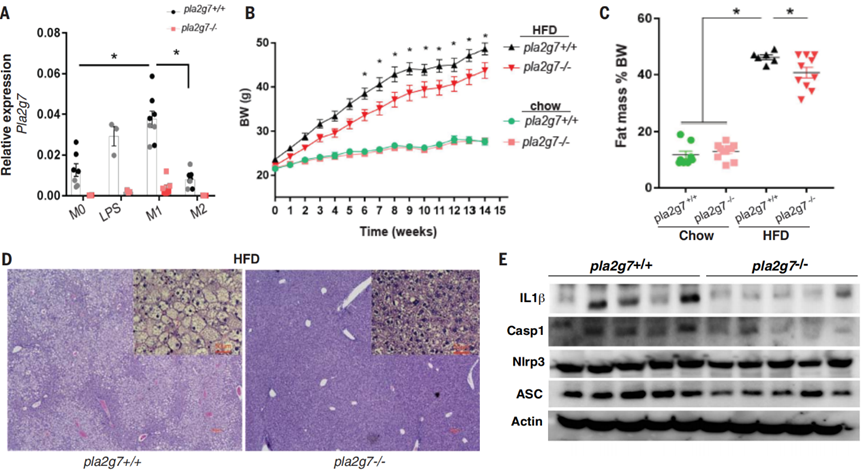
Pla2g7基因表达缺失改善了小鼠脂肪代谢
另一方面,Pla2g7基因敲除缓解了小鼠的胸腺随年龄增大而发生的退化。与野生型24个月大的老年小鼠(≈人类70岁)相比,Pla2g7基因敲除的老年小鼠胸腺体积更大,T细胞丰度更高。
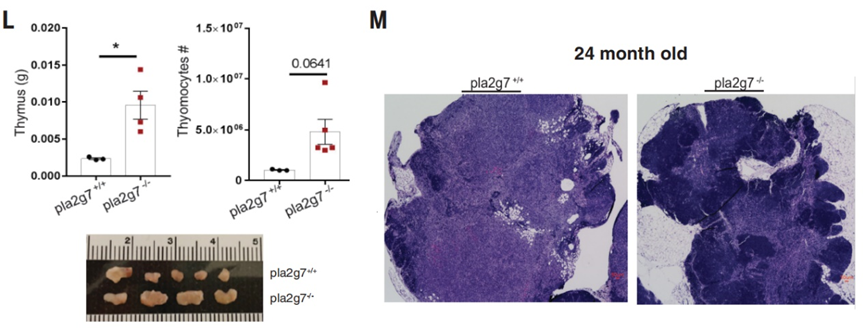
Pla2g7基因表达缺失的老年小鼠胸腺功能恢复
总体来说,Dixit和他的同事们根据迄今为止最大的人类热量限制队列研究分析得出,坚持长期热量摄入减少14%有助于恢复胸腺功能,增大胸腺体积、提高胸腺产生T细胞的能力,从而改善随年龄增长而出现的免疫功能衰退。
不仅如此,研究者们证实PLA2G7基因在脂质代谢和炎症反应中的作用, 并在小鼠身上发现,Pla2g7基因缺失的效果与热量限制带来的健康益处相近。
他们认为,未来或许可以Pla2g7基因为线索,模拟热量限制,从而改善人体脂肪组织代谢、降低炎症反应、减少胸腺脂肪萎缩等。
总之啊,热量限制它真的是人间值得!
所以,到底还得说多少遍热量限制对健康延寿的益处,才能坚持管住这张嘴,而不是“下顿饭吧”“明天吧”“下周再开始”呢?!
参考文献:
[1]https://www.science.org/doi/10.1126/science.abg7292#
[2]J. Rochon, et al; CALERIE Study Group, Design and conduct of the CALERIE study: Comprehensive assessment of the long-term effects of reducing intake of energy. J. Gerontol. A Biol. Sci. Med. Sci. 66, 97–108 (2011).
[3]Martin CK, Bhapkar M, et al. Effect of Calorie Restriction on Mood, Quality of Life, Sleep, and Sexual Function in Healthy Nonobese AdultsThe CALERIE 2 Randomized Clinical Trial. JAMA Intern Med.2016;176(6):743–752.
[4]Ravussin E, et al; CALERIE Study Group. A 2-Year Randomized Controlled Trial of Human Caloric Restriction: Feasibility and Effects on Predictors of Health Span and Longevity. J Gerontol A Biol Sci Med Sci. 2015 Sep;70(9):1097-104. doi: 10.1093/gerona/glv057.
[5]W. E. Kraus, et al; CALERIE Investigators, 2 years of calorie restriction and cardiometabolic risk (CALERIE): Exploratory outcomes of a multicentre, phase 2, randomised controlled trial. Lancet Diabetes Endocrinol. 7, 673–683 (2019).
[6]Dixit VD. Thymic fatness and approaches to enhance thymopoietic fitness in aging. Curr Opin Immunol. 2010 Aug;22(4):521-8. doi: 10.1016/j.coi.2010.06.010.
[7]https://www.science.org/doi/10.1126/science.abn6576
本文来自微信公众号:奇点网(ID:geekheal_com),作者:张艾迪