

扫码打开虎嗅APP
本文来自微信公众号:返朴(ID: fanpu2019),作者:史隽,题图来自:视觉中国
防护依旧是目前不能松懈的工作,而消毒剂也是离不开的。一种好的消毒剂,要在对人体和环境的危害可以接受的浓度范围内,快速杀死病毒。那么,我们该如何挑选消毒剂?挑选时要注意什么呢?
3月17日,《新英格兰医学杂志》(The New England Journal of Medicine)发表了一篇来自美国科学家的通讯 (Correspondence),研究了新冠病毒 (SARS-CoV-2) 在气溶胶中和在各种环境表面的存活时间,并与SARS冠状病毒 (SARS-CoV-1)相比较[1],还用贝叶斯回归模型估算了病毒活性的衰减速度。

该文数据包括这两个病毒在温度为21℃至23°C,相对湿度为40%的五个环境中的存活时间。五个环境分别为:直径小于5微米的气溶胶中、塑料表面、不锈钢表面、铜表面和纸板表面。
病毒的滴度直接决定病毒的感染能力,也决定了病毒失去活性的难易程度。浓度越高,越容易导致感染,失活越难。如果用核酸检测法来定量的话,该文选用的病毒的起始滴度和病人呼吸道中观察到的相似。
结果用一张图全部概括了:

图1:SARS-CoV-1(SARS冠状病毒)和SARS-CoV-2(新冠病毒)在气溶胶和各种环境表面上的稳定性 (来源于参考文献[1])。(点击看大图)
总结下来就是:
在气溶胶中,新冠病毒与SARS病毒的观察结果相似:在整个实验过程(3个小时)中都能检测到有感染力的病毒,感染滴度略有降低 (幅度约为1log10)。
新冠病毒在不同环境表面的稳定性排名是:塑料 > 不锈钢 > 纸板 > 铜表面。
在塑料表面, 有感染力的新冠病毒可以存在72小时。在不锈钢表面,可以存在48小时。但是有感染力的病毒滴度降低很明显。
在铜表面,4小时后就检测不到有感染力的新冠病毒了。在纸板上,24小时以后检测不到有感染力的新冠病毒。
用一个更直观的图来表示如下:
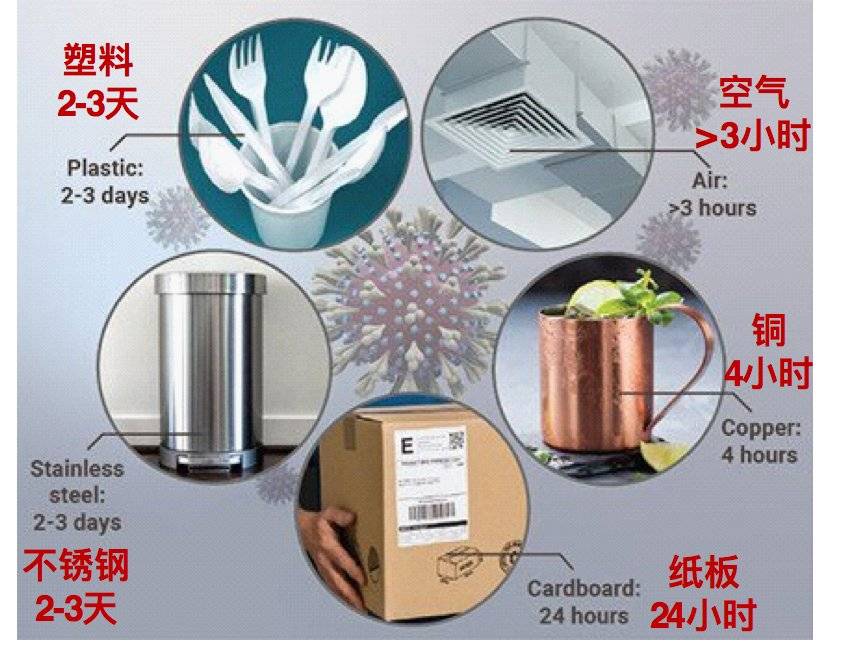
图2:新冠病毒 (SARS-CoV-2) 在环境表面的存活时间 (修改原图https://www.medscape.com/viewarticle/926929)。
另一个新的研究,用的病毒起始滴度较高,结果也类似[2],在室温(22°C)、相对湿度约为65%的环境下:
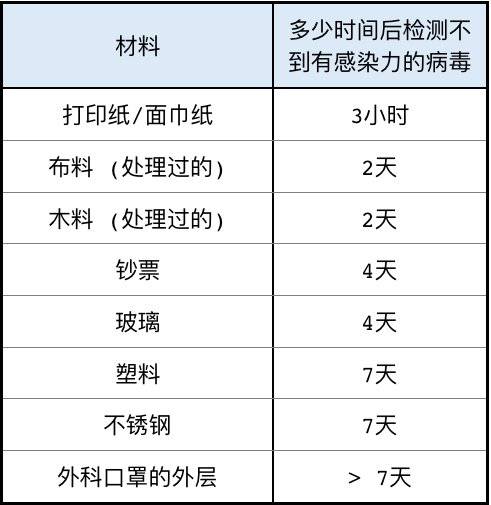
关于冠状病毒,还有两点补充:
pH值对冠状病毒的影响:大多数冠状病毒在弱酸性(pH=6~6.5)下比碱性(pH=8)下更稳定 [3-7]。
在粪便中,可检测到新冠病毒存在。根据对SARS病毒的研究,在成年人的正常粪便中,SARS病毒不能存活超过24小时;而在新生儿的粪便中(pH值酸性),存活时间不能超过3小时。然而,它在pH值可能达到9的腹泻粪便中可以存活很长时间,最多可达4天 [8]。
同时,一个新的研究发现,48.5%的COVID-19病人有消化系统症状,如腹泻、呕吐和腹痛等 [9]。因此对可能患有新冠肺炎的病人,其腹泻粪便一定要及时小心处理。
虽然到底病毒的浓度要达到多少会引起感染还没有结论,但是这些结果表明,新冠病毒很有可能通过气溶胶 (在高浓度病毒条件下的小概率事件) 和接触传播。
新冠病毒从被污染的环境表面转移到手上的效率有多高?暂时还没有看到数据。但是,对甲型流感病毒的研究表明,只要接触被污染的环境表面5秒钟,就会有31.6%的病毒载量转移到手上[10]。
再次提醒:大家手部卫生非常重要!
口罩对于预防飞沫喷溅到口咽鼻来说很重要,但口罩不是万能的。如果能好好洗手和给环境做好消毒,就能预防大部分的接触传播。洗手的重要性和正确洗手的方法在前面的文章里已经说过了,在这里不再重复阐述了。那么,消毒应该怎样操作?市面上有各种各样五花八门的消毒剂,大多打着 “能杀死99.9%的病菌”的标签。这些消毒产品都对新冠病毒有用么?使用消毒产品有哪些注意事项?
消毒剂——不论是用于给身体消毒 (英文叫做antiseptic)还是用于给环境消毒 (英文叫做disinfectant)——到底有没有用,需要进行严谨的有效性测试。
测试通常是4步:1) 混合;2) 中和;3) 回收;4) 定量。首先将病毒和待测试的消毒剂混合,经过一段时间后,人为快速有效地中和消毒剂的活性和毒性,然后测量剩下的有感染力的病毒的滴度 (titre, 就是一定体积中的病毒数量)。
中和有几种方法,例如稀释中和(neutralization by dilution),化学物质中和(chemical neutralization)和凝胶过滤(gel filtration),各有优点和局限性。
为什么要快速有效地中和消毒剂的活性和细胞毒性?
1) 为了精确控制病毒和消毒剂接触的时间。不论什么方法,灭活病毒都需要时间。这个时间可以很短,低于30秒;也可能很长,需要几天。一种好的消毒剂,要在对人体和环境的危害可以接受的浓度范围内,快速杀死病毒。通常我们只会选择接触时间 ≤ 1分钟的消毒剂。
2) 定量有感染力的病毒的滴度,方法是看病毒杀死宿主细胞的能力。然而,测试终止的时候,消毒剂和病毒仍然是充分混合在一起的。如果不去除掉消毒剂的细胞毒性,那么消毒剂也会杀死宿主细胞,而不是只是有感染力的病毒可以。最终病毒的滴度的结果就会很不准确。
中和以后,还要有一个好方法成功回收未被消毒剂杀死的病毒,才能进行下一步剩下的病毒定量。
病毒定量是将病毒和宿主细胞混合,过一定时间以后,观察病毒对细胞造成的病变效用 (cytopathic effect)来计算有感染细胞能力的病毒的量。细胞病变效应是指病毒入侵后,在宿主细胞中引起的结构变化,有多种不同的表现形式,常见的有被感染的细胞变圆了,极端的就是细胞被病毒杀死了。
一个好的测试,还要尽可能地模拟产品未来会被使用的条件。因此存在不同类型的测试,提供的数据也不同,例如:
悬浮液测试 (suspension tests):病毒和消毒剂悬浮混合,可用于筛选不同化学成分杀灭病毒的效率和对宿主细胞的毒性;
载体测试 (carrier tests):把病毒滴在不同物质的表面上,看消毒剂对这些已经干燥了的病毒的作用。
现场测试 (in-field tests),例如在医院环境中。由于成本和标准化问题,这个测试很少做。
在所有这些测试中,有时候还会添加一些有机载体(血清、粪便、蛋白等)。这是因为:
1) 现实生活中,病毒通常是被这些载体包围的。
2)载体有时候能保护病毒免受消毒剂的作用。
3)大部分消毒剂 (例如含氯的化合物) 会被这些有机载体灭活。
4)病毒会自行聚集,而有机载体会增强病毒的聚集,使它们对消毒剂更具有抵抗力。
根据美国监管机构的标准,如果消毒剂在明确定义的接触时间内,可以让有感染力的病毒滴度降低3 log10以上,就可以认为该消毒剂具有有效的杀病毒活性[11]。而欧洲的监管机构则要求可以降低4log10 以上[12]。
用通俗的广告词来说,降低高于3log10的病毒滴度,就是能杀死99.9%的病毒;降低高于4log10的病毒滴度,就是能杀死99.99%的病毒。
因此,挑选消毒剂最需要注意的是两点:
1)消毒剂的成分
2)需要的接触时间
成分大家很容易理解,不同化学物质对病毒的灭活作用不同。而另外一个指标“接触时间”则经常被大家忽略。所谓“需要的接触时间”就是指病毒需要和这些消毒剂接触至少多久,其有感染力的滴度才能被有效地降低。
如果仔细看消毒剂的包装,通常很多在后面会有成分和 “contact time (接触时间)”。

图3:美国常见的一种lysol消毒喷雾。也许是因为酒精含量比较低 (58%),和病毒的接触时间需要比较长。

图4:国内常见的84消毒液的参数
虽然现在还没有针对新冠病毒的消毒剂数据,但是有一些针对别的冠状病毒的数据可以借鉴。
有一篇文章总结了美国市面上常见的消毒剂成分对冠状病毒的灭活作用[13]。
(一)
第一个结果比较了不同成分在载体测试中对一个普通的人冠状病毒229E的灭活作用[14]。
结果见下表,大家可以检索自己家里有的消毒剂是不是管用 (有效 “Yes” 被定义为1分钟的接触时间后病毒滴度降低≥3log10)。

图5:各种常见的消毒剂成分在载体测试中对人冠状病毒229E的灭活效果[14]。
通常认为,有脂质包膜的冠状病毒不是很稳定,应该能很容易被灭活。然而,这个研究发现并不是这样。许多季铵化合物 (quaternary ammoniums compounds)或酚类化合物 (phenolic compounds) 之类的消毒剂对它无效。
(二)
另一个研究总结了一些消毒剂在悬浮液测试中对SARS冠状病毒(SARS-CoV-1)的灭活作用[15]。
研究发现,大多数酒精类的消毒剂 (异丙醇或乙醇)在≥70%的浓度能在30秒内降低 > 4log10的病毒滴度,不管有没有有机载体。

图6:各种常见的消毒剂成分消毒剂在悬浮液测试中对SARS-CoV-1的灭活作用[15]。
(三)
另一项发表在《医院感染杂志》上的文章[16]总结了好几个研究,发现类似于新冠病毒的其他冠状病毒可以被以下几种消毒剂在1分钟内“有效”地灭活:
含有70%以上的酒精 (ethanol)或者异丙醇 (isopropanol)。
0.5%的过氧化氢(hydrogen peroxide)。
0.1%次氯酸钠 (sodium hypochlorite,就是我们俗称的漂白剂/bleach,也是84消毒液的主要成分)的消毒剂[16]。
虽然对于新冠病毒还没有确实的数据,研究人员推论这些消毒剂应该也有类似的效果。
这里有三点要提醒大家注意:
1)有些研究发现低于70%的酒精类 (例如62%的浓度) 在载体测试中能有效杀死两个动物冠状病毒,而另外的研究发现其只对一种动物冠状病毒有效。结果不很一致。为了安全起见,建议使用70%以上的浓度。
2)次氯酸钠 (sodium hypochloride) 要高于0.1%的浓度才对冠状病毒有效。通常漂白剂 (bleach) 里面次氯酸钠的浓度是5%,因而应该稀释1:50使用,而不是通常建议的1:100稀释。84消毒液里面有效氯含量5.5~6.5%,也是1:50稀释使用。
3)消毒剂对环境和健康都是有一定危害的。例如,次氯酸钠进入水中,就会与其他化学物质发生反应,形成二恶英 (dioxin) 等产物。二恶英是会对健康造成严重影响的毒素,对水生物有害。生产乙醇过程会产生和排放温室气体二氧化碳(CO2)。能够节约使用还是少用,使用最低有效浓度把对人体有可能的毒性降到最低。
最后,一定要注意,切勿随意将家用清洁剂混合!
将清洁剂混合在一起有时会产生有毒气体。例如,将漂白剂与酸性溶液混合,会发生化学反应,产生氯气,刺激眼睛、喉咙和鼻子。高浓度的氯气会导致呼吸困难和肺部积液,非常高浓度的时候甚至会导致死亡。
下面的图就举例了几种常见的消毒液混合以后会产生的后果。

图7:常见的消毒液混合以后会产生的后果 (原图来自于美国加州滨江县 Riverside County消防局的tweeter)
参考文献
[1] N. van Doremalen et al., Aerosol and Surface Stability of SARS-CoV-2 as Compared with SARS-CoV-1. New England Journal of Medicine, (2020).
[2] A. W. H. Chin et al., Stability of SARS-CoV-2 in different environmental conditions. The Lancet Microbe.
[3] A. Lamarre, P. J. Talbot, Effect of pH and temperature on the infectivity of human coronavirus 229E. Canadian Journal of Microbiology 35, 972-974 (1989).
[4] B. D. Zelus, J. H. Schickli, D. M. Blau, S. R. Weiss, K. V. Holmes, Conformational Changes in the Spike Glycoprotein of Murine Coronavirus Are Induced at 37°C either by Soluble Murine CEACAM1 Receptors or by pH 8. Journal of Virology 77, 830-840 (2003).
[5] C. Daniel, P. J. Talbot, Physico-chemical properties of murine hepatitis virus, strain A 59. Brief report. Arch Virol 96, 241-248 (1987).
[6] D. H. Pocock, D. J. Garwes, The influence of pH on the growth and stability of transmissible gastroenteritis virus in vitro. Arch Virol 49, 239-247 (1975).
[7] A. Pratelli, Canine coronavirus inactivation with physical and chemical agents. The Veterinary Journal 177, 71-79 (2008).
[8] M. Y. Y. Lai, P. K. C. Cheng, W. W. L. Lim, Survival of Severe Acute Respiratory Syndrome Coronavirus. Clinical Infectious Diseases 41, e67-e71 (2005).
[9] M. M. Lei Pan, Pengcheng Yang, Yu Sun, Runsheng Wang, Junhong Yan, Pibao Li, Baoguang Hu, Jing Wang, Chao Hu, Yuan Jin, Xun Niu, Rongyu Ping, Yingzhen Du, Tianzhi Li, Guogang Xu, Qinyong Hu, Lei Tu, Clinical characteristics of COVID-19 patients with digestive symptoms in Hubei, China: a descriptive, cross-sectional, multicenter study. The American Journal of Gastroenterology, (2020).
[10] B. Bean et al., Survival of Influenza Viruses on Environmental Surfaces. The Journal of Infectious Diseases 146, 47-51 (1982).
[11] http://microchemlab.com/test-category/virucidal-efficacy-testing.
[12] AFNOR, Chemical disinfectants and— Virucidal quantitative suspension test for chemical disinfectants and antiseptics used in human medicine — Test method and requirements (phase 2, step 1). NF EN 14476+A1., (2007).
[13] C. Geller, M. Varbanov, R. E. Duval, Human coronaviruses: insights into environmental resistance and its influence on the development of new antiseptic strategies. Viruses 4, 3044-3068 (2012).
[14] S. A. Sattar, V. S. Springthorpe, Y. Karim, P. Loro, Chemical disinfection of non-porous inanimate surfaces experimentally contaminated with four human pathogenic viruses. Epidemiol Infect 102, 493-505 (1989).
[15] H. F. Rabenau et al., Stability and inactivation of SARS coronavirus. Med Microbiol Immunol 194, 1-6 (2005).
[16] G. Kampf, D. Todt, S. Pfaender, E. Steinmann, Persistence of coronaviruses on inanimate surfaces and their inactivation with biocidal agents. Journal of Hospital Infection 104, 246-251 (2020).
本文来自微信公众号:返朴(ID: fanpu2019),作者:史隽
