

扫码打开虎嗅APP
本文来自微信公众号:机器之能(ID:almosthuman2017),作者:吴昕,题图来自:IC photo
4月26日,深圳妇幼保健院生殖医学中心主任李雪梅等,在预印本网站bioRxiv上传了一篇尚未经同行评议的论文,题为《GS-5734对雄性小鼠生殖毒性的一项初步研究》(A preliminary study on the reproductive toxicity of GS-5734 on male mice),GS-5734即尚未正式获批上市的瑞德西韦的研发代号。
初步研究显示,瑞德西韦可能对小鼠形成生殖毒性,造成总精子数和活动精子率显著下降,异常精子率增加。
虽然这项研究尚未经过同行评议,不过仍然具备一定警醒价值。当年非典期间,为了抢救生命,激素类药物曾被大量用于非典紧急治疗,病人痊愈后,引发一系列后遗症,如骨质疏松、股骨头坏死、肺纤维化等。
非典股骨头坏死后遗症患者接受治疗
据当年对110名非典后遗症患者做的问卷调查中,超过70%的人因为股骨头坏死接受相关治疗,超过60%的人因肺纤维化接受相关治疗,因后遗症而丧失工作能力或生活自理能力的人超过1/3。
17年后,一样被誉为“人民的希望”的瑞德西韦,前车之鉴下,我们对于其可能产生的后遗症、副作用等需要前置思考,一旦这项研究经过同行评议,得到证实,不仅研发瑞德西韦的吉利德公司股价会受到影响,之前普遍的临床治疗所带来的后遗症更是无尽的麻烦。
一、可引起小鼠睾丸毒性
瑞德西韦是一种核苷酸类似物前药,能够竞争地结合并抑制依赖RNA的RNA合成酶(RdRp)。
不过,核苷酸类似物可能对配子产生、胚胎发育和性腺功能具有潜在毒性。例如,嘌呤类化合物就与激素分泌、勃起、精子运动和获能相关。
在此背景下,论文研究人员参考现有文献合成了GS-5734,通过氢谱核磁共振和质谱仪检验过结构和纯度后进行生殖毒性试验。
研究人员将28只成年雄性C57小鼠随机分为4组(每组7只),以1组为对照组,1、2、3、4组分别每日每只腹腔注射0μg、10μg、50μg、150μg的GS-5734,持续10天。小鼠体重在22克上下,以体重换算,50ug的中剂量组比较接近人类用量。
最后一次注射后第7天,对小鼠用二氧化碳吸入的方式处死,取左附睾尾切片获得精子样本,制备成精子悬液后,研究人员进行染色后,以400倍放大检测每只小鼠的200多个精子,观察精子形态和精子活力。
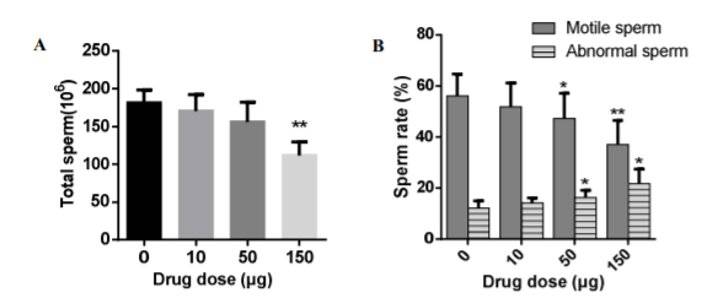
各组小鼠总精子数、活动精子率和正常精子率
右侧睾丸和附睾则予以手术摘取,除去脂肪,切片染色后在显微镜下拍摄睾丸生精上皮结构和储存在附睾中的精子变化。
结果显示,经GS-5734处理后,小鼠的总精子数和活动精子率呈下降趋势,异常精子率呈上升趋势。
与对照组相比,GS-5734日剂量150μg的小鼠精子浓度和运动能力显著降低,异常精子率显著升高;日剂量50μg的小鼠精子运动能力显著降低,异常精子率升高。
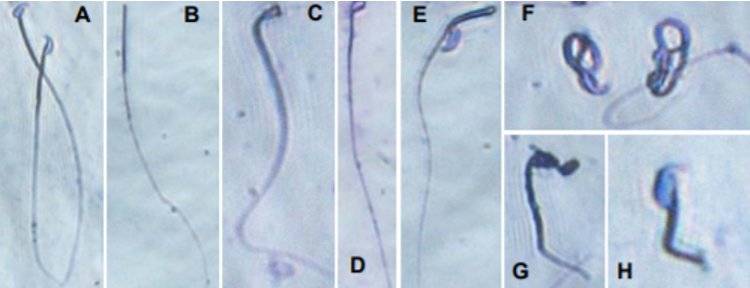
A 对照组的正常精子;B-H组 为药物组出现的异常精子,包括无头、小头、头部畸形、体部畸形、尾部畸形、整体畸形
睾丸和附睾组织HE染色经GS-5734处理后,小鼠的总精子数和活动精子率呈下降趋势,异常精子率呈上升趋势显示,随着GS-5734剂量的增加,小鼠精子发生明显恶化。
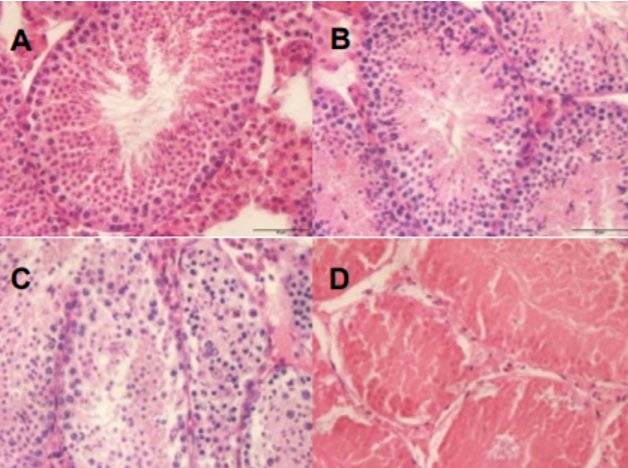
实验组小鼠睾丸染色切片:A为10 μg组、B为50 μg组、CD为150μg组
10μg/只小鼠组的睾丸功能未出现明显变化;
50μg/只小鼠组出现轻微变化,生精管内有许多晚期精细胞和精子,排序紊乱,腔内有脱落的生精细胞;
150μg/只小鼠组出现明显变化,晚期精细胞和精子大量减少甚至消失,早期精细胞减少或消失,睾丸组织和细胞结构的纤维化消失。
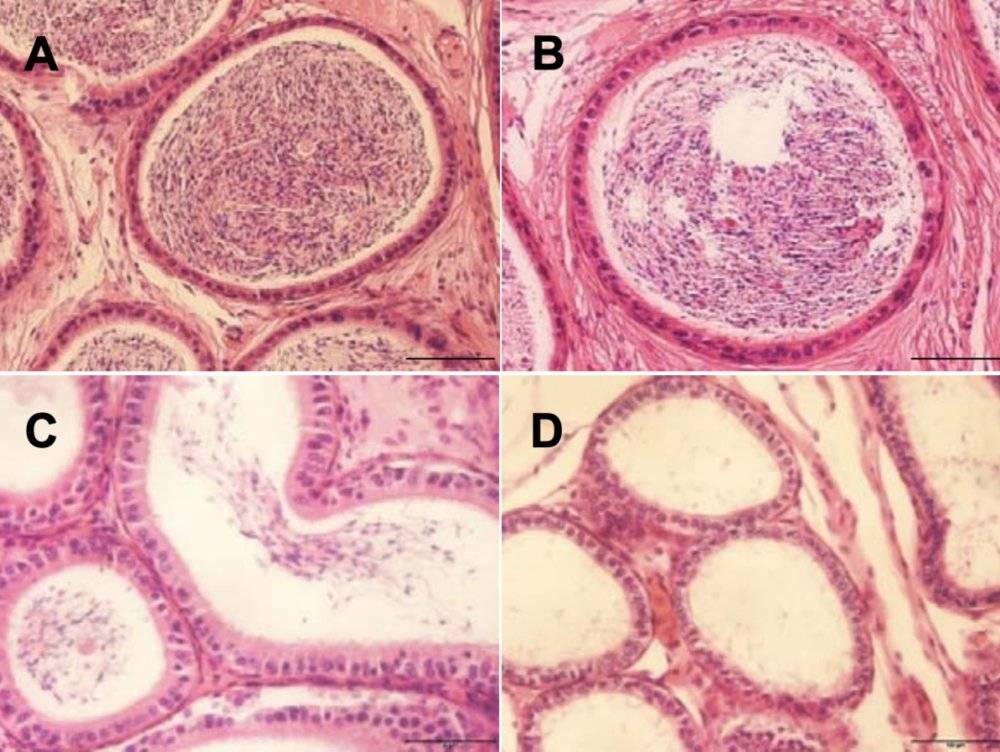
实验组小鼠附睾组织染色切片:A为10 μg组、B为50 μg组、CD为150μg组
10μg/只小鼠组的附睾管中有高浓度的精子;
50μg/只小鼠组的附睾管中精子浓度略有降低,但总浓度仍高;
150μg/只小鼠组的附睾管中精子浓度明显降低,甚至不可见(D)。
作者团队因此得出结论,高剂量瑞德西韦可引起小鼠睾丸毒性,导致雄性小鼠的精子参数下降。
在比较接近人类常规使用浓度的中剂量实验组中(50ug一组),小鼠也出现了睾丸生精功能轻微改变、精子活力显著下降,异常精子率提高。这暗示着,患者在接受治疗后可能需要一段时间来恢复生精功能,确保生殖安全。
目前,海外疫情仍在持续蔓延,如果瑞德西韦作为一线治疗药物在国际上得到广泛应用,那么关于它的生殖毒性还需要更深入的研究。
二、“人民的希望”瑞德西韦质疑不断
吉利德吉创立于1987年6月22日,总部位于美国加州福斯特城。作为生物制药公司,其主要致力于医疗需求未得到满足领域的药物研究、开发及商业化,重点研究领域包括人类免疫缺陷病毒、后天免疫缺陷综合症(AIDS)等。
瑞德西韦是吉利德科学公司正在研发的一种新型实验性广谱抗病毒药物。虽在埃博拉临床试验失败,但瑞德西韦仍可以有效抑制呼吸道上皮细胞中SARS病毒和MERS病毒的复制。
基于“同情用药”原则,美国研究人员今年1月对一名新冠肺炎患者使用了瑞德西韦,患者症状在一两天内显著改善,使这种药物备受关注,后续来自全球100多个临床试验站点的2400名重症病患试验,都在积极推动瑞德西韦的临床试验。

不过,近日来瑞德西韦风波不断。4月11日,NEJM(新英格兰医学杂志)发布瑞德西韦进入新冠肺炎后的首个临床研究结果。
53名来自美国、欧洲、加拿大及日本的严重和危重新冠肺炎患者中,总计36人(68%)症状有改善,但有12名(23%)患者出现严重副作用,包括多器官功能障碍综合征、败血性休克、急性肾损伤和高血压。
受此消息影响,截至当地时间4月15日收盘,吉利德科学股价跌4.01%,报收74.63美元。
后续一波未平一波又起,4月24日,瑞德西韦在中国进行的一项临床试验结果遭WHO意外提前披露,与标准治疗对照组相比,瑞德西韦与“临床改善时间的差异无关”。
据了解,这是一项在中国进行的随机3期临床试验,共计入组237名新冠肺炎重症患者,其中158例为瑞德西韦给药组,79例为对照组,但最后用药组中有18例、对照组中有4例因副作用停止治疗。
数据显示,给药组死亡率略高(治疗组为13.9%,对照组12.8%)、不良反应率略高(治疗组为65%,对照组为64%),这也意味着瑞德西韦并未改善新冠肺炎患者预后。
这一消息的披露更是让吉利德股价一度下跌8.5%,成为3月16日以来的最大跌幅。
上市之前瑞德西韦已历经种种风波,而一般而言新药即使经过第三期临床试验后,药品审批还须经过半年到两年时间方可正式上市,目前瑞德西韦最终获准上市的时间仍待定。
关于未来进一步临床结果披露,吉利德首席医疗官Merdad Parsey表示,公司将在4月底公布其开展的瑞德西韦用于治疗重症新冠肺炎的随机开放研究结果;5月底公布瑞德西韦用于治疗重症新冠肺炎患者的开放试验研究,以及公布美国国家过敏和传染病研究所(NIAID)对不同疾病严重程度患者进行的瑞德西韦双盲安慰剂对照试验数据。
而有关瑞德西韦的后遗症、副作用,要等到更多的临床试验和学术研究来揭示,此次深圳妇幼保健院生殖医学中心的小鼠实验或许只是一个开头。
参考内容:
1.https://www.biorxiv.org/content/10.1101/2020.04.21.050104v1.full.pdf
2.https://www.thepaper.cn/newsDetail_forward_7140013
本文来自微信公众号:机器之能(ID:almosthuman2017),作者:吴昕,题图来自:IC photo
