

扫码打开虎嗅APP
本文来自微信公众号:量子位(ID:QbitAI),作者:金磊、明敏,头图来自:视觉中国
CRISPR-Cas9这把“基因剪刀”,到底该归谁?
针对这场旷日持久的“拉锯战”,美国专利商标局做出了最新裁决——
张锋团队击败诺奖得主,拥有优先权。

换言之,此次判决承认了张锋所在的Broad团队,是第一个发明CRISPR-Cas9来编辑人类细胞并用于制造药物的团队。

图片来自:MIT
而与之争锋的CVC团队,即便有着两位诺奖得主(Jennifer Doudna 和 Emmanuelle Charpentier)坐镇,依旧失利于此次判决。
要知道,此前她们正是因为在CRISPR-Cas9方面的突出贡献,而获得2020年诺贝尔化学奖。
当时也有许多人对于张锋无缘诺奖而唏嘘不已。
但这一次,美国专利商标局对此给出的理由是:
CVC未能提供充分、有力的证据,证明他们领先于Broad团队。
因此,拒绝CVC关于不公平行为的论点,拒绝CVC在本诉讼中涉及的权利要求。
这也就意味着,张锋所创立的基因编辑公司Editas Medicine,可以在美国可获得涵盖所有人类细胞的CRISPR-Cas9和CRISPR-Cas12a的基因编辑专利。
相对的,这项裁决对于CVC团队所在的加州大学伯克利分校来说可谓是损失惨重。
外媒对此评价道:
其在美国的许可收入可能损失1亿至100亿美元。

“基因剪刀”,为什么判给了张锋?
下面,我们来看一下专利判决书中的具体内容。
上诉委员会判定,在“CRISPR-Cas9于真核细胞中的应用”这一专利上,CVC团队与之相关的9项技术不再具有专利权。
判决书中表示,争论的焦点在于“谁先发明了CRISPR-Cas9系统中在真核细胞应用中的单向导RNA”。
这种单向导RNA上携带一种酶,是靶向编辑DNA、影响基因表达的关键。
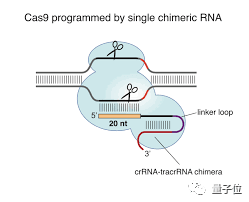
更重要的是,在真核细胞中的基因编辑对开发人类药物的影响十分深远,这也是此次专利之争为什么会引起广泛关注的原因之一。
比如肥厚型心肌病、镰状细胞性贫血等遗传疾病的治疗,都受到CRISPR技术的影响。
全球众多生物技术、制药公司都在使用CRISPR作为核心技术开发新疗法。
由此,受到这次专利之争的影响,许多此前从CVC方面获取专利使用权的公司,将必须重新与Board方面重新签订协议。
这将是一笔巨大的损失。因为这些企业在此前的临床试验中已经取得了突破,之后的专利授权费可能会水涨船高。
当然还有目前最直接的影响——股价。
比如与诺华、再生元都有合作关系的Intellia公司,此前就是与CVC方面获取专利许可,目前它们的股价已经下跌19.22%。
但如果此前“押注”Board团队,局面就会是另一种形态了:
与Board方面获取专利许可的生物技术公司Editas Medicine Inc.,则在周一收盘前股价上涨17%。
不过这场漫长的专利之争,还只是暂时性地画上了句号。
因为这次胜诉只意味着CVC团队之后不可以干涉Board在美的专利使用权,其他地区的专利到底属于谁,还并没有尘埃落定。
事实上,在欧洲方面CVC团队或许略胜一筹。
截至2018年,欧洲专利局已经正式授予给CVC坐镇的Emmanuelle Charpentier两项关于CRISPR-Cas9的专利。
一场持续数年的“专利战”
这场“专利战”所围绕的一个核心技术,便是CRISPR-Cas9。
CRISPR,是Clustered Regularly Interspaced Short Palindromic Repeats(成簇规律间隔短回文重复序列)的缩写。
简单来说,CRISPR是微生物体内的一种天然“免疫系统”,当病毒侵入细菌的时候,就可以通过它来产生“记忆”。
CRISPR最早是在20世纪80年代,由日本科学家发现。
直到Emmanuelle Charpentier和Jennifer Doudna找到了Cas9这种蛋白(链球菌用于免疫防卫的酶)之后,其基因组编辑工具的巨大潜力才逐渐被挖掘出来。
这是因为酶在基因编辑的过程中,相当于一种“分子剪刀”,可以在特定的位点切断双链DNA。
在DNA断裂之后,细胞会对断裂位点进行修复。
但在此之前,科学家们在这个过程往往会遇到一个痛点,那就是每修饰一次基因,就需要针对想要修饰的DNA序列设计一种新的蛋白。
而Cas9就不一样了,它会用RNA来引导自己,在DNA上不停“扫描”,直到找到正确的位点。
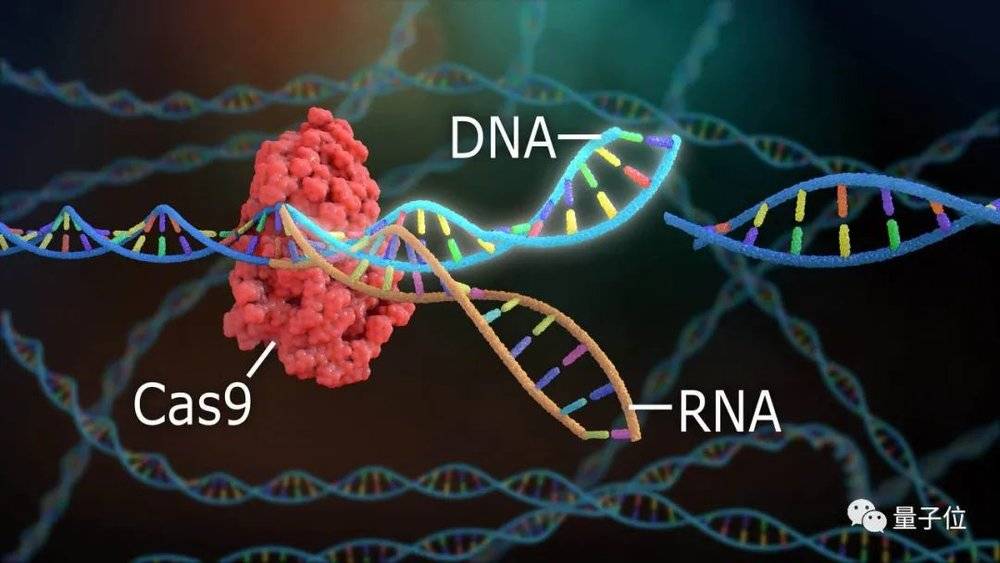
于是,她们便做出了这样的设想:
可以将这些RNA分子设计成一条gRNA。
一套由一个蛋白质和一条gRNA组成的系统,就足以成为一个强大的基因修饰工具。
通过实验,她们的设想还真的取得了成功——成功在试管和细菌体内实现了CRISPR的基因编辑。
于是在2012年,Charpentier和Doudna便将CRISPR-Cas9的研究成果在Science上公诸于众。

或许以她们的实力,实现CRISPR在动物体内的基因编辑只是时间问题。
而一上升到动物这一层面,这个技术便可以在医疗(探索艾滋病、阿尔茨海默病、精神分裂症等疾病的治疗方法)、科研、农业等领域完全铺展开来,大展拳脚。
换言之,其他人便很难再去染指CRISPR的核心利益。
就在这时,张锋所带领的团队于2013年同样在Science上发表论文,并宣告:
成功利用CRISPR系统编辑了动物的基因。

也就是说,前者解析了工作原理,后者则是将它应用到了哺乳动物身上。
二者所做出的工作对业界产生的影响力都极为轰动。
但在奖项方面,张锋团队却属于较为“失意”的一方。
例如2020年的诺贝尔化学奖,便颁给了Charpentier和Doudna,张锋与之无缘。

而更早的,像2020年度的沃尔夫奖生物学奖、2016年阿尔珀特奖、2015年科学突破奖,也均是颁给了Charpentier和Doudna。
不过张锋团队在专利上,所得到结果却截然不同。
Charpentier和Doudna是在2012年5月提交了专利申请,而张锋团队则是在同年12月提交。
毕竟CRISPR-Cas9背后的商业价值可谓是不可估量,这场“专利拉锯战”也就逐渐拉开了序幕。
2014年,美国专利商标局先批准了张锋团队的专利申请。
这下,Charpentier和Doudna所在的CVC团队就不乐意了——“我们先发现的CRISPR-Cas9,专利也是先提交的”。
于是在2016年,CVC团队便向美国联邦法院上诉,但结果却是被驳回。
而到了2017年,美国专利商标局给予了张锋团队在这场“拉锯战”中,极为关键的判决:
批准专利不做更改。
时至今日,美国专利商标局最新裁决,依旧是倾向于张锋团队。
……
可以说,张锋团队虽然在奖项“失意”,但在专利上却是“得意”的一方了。
张锋是谁?
那么这次事件的主角——张锋到底是谁?

图片来自:McGovern Institute, MIT
张锋,1982年出生于河北石家庄,11岁随家人移居美国。
2004年,张锋于哈佛大学本科毕业,2009年在斯坦福大学获得化学及生物工程学博士学位,师从光遗传学之父卡尔·迪赛罗丝。
在研究生阶段,他便与团队一起开发出了利用光激活大脑神经元的技术,揭示了精神分裂症、双相情感障碍等疾病的根源。
最负盛名的当然还是他在CRISPR方面的工作。
2011年,在一次学术会议上,张锋听到了关于CRISPR方面的研究,当时这一技术的相关文献不多,关注的应用场景是CRISPR是否能帮助生产出更好的酸奶。
在后来的采访中,张锋透露他当时便想到:
我们能让它在人类细胞中工作吗?
由此,也就开启了张锋在CRISPR方面的多年探索。
2013年,其名震业内的成果《利用CRISPR/Cas系统进行多重基因组工程》在Science上发表。
之后第二年,他被Nature评选为“2013年年度十大科学人物”之一。后来被业内称为CRISPR三巨头之一。
在当初Charpentier和Doudna因为在基因编辑方面的卓越贡献获得诺奖时,不少人为张锋的落选表示惋惜。
2021年,张锋当选美国国家医学科学院院士。
入选理由是:通过发现新型微生物酶和系统及其作为分子技术的发展(如光遗传学和CRISPR基因编辑),彻底改变了分子生物学,并推动研究和治疗人类疾病的能力实现变革性飞跃,以及对其出色的指导和专业服务。
……
最后,这场“专利战”的全盘结局将如何发展,还需拭目以待。
参考链接:
[1]https://www.mercurynews.com/2022/02/28/uc-berkeley-loses-crispr-gene-editing-patent-case/
[2]https://www.scribd.com/document/561762623/106-115-Decision-on-Priority
[3]https://mp.weixin.qq.com/s/glN5z7oj-m2fWUpKZ4eO_w
本文来自微信公众号:量子位(ID:QbitAI),作者:金磊、明敏
